高中化学喷泉实验长沙克立兹外国语学校是一所专业从事高考文化补(12)
SO2(过量)+NaOH=NaHSO3(SO2+OH-=HSO3-)
b、与Ca(OH)2溶液反应:
SO2(少量)+Ca(OH)2=CaSO3↓(白色)+H2O
2SO2(过量)+Ca(OH)2=Ca(HSO3) 2 (可溶)
对比CO2与碱反应:
CO2(少量)+Ca(OH)2=CaCO3↓(白色)+H2O
2CO2(过量)+Ca(OH)2=Ca(HCO3) 2 (可溶)
将SO2逐渐通入Ca(OH)2溶液中先有白色沉淀生成,后沉淀消失,与CO2逐渐通入Ca(OH)2溶液实验现象相同,所以不能用石灰水来鉴别SO2和CO2。能使石灰水变浑浊的无色无味的气体一定是二氧化碳,这说法是对的,因为SO2是有刺激性气味的气体。
②so2能与酸性高锰酸钾溶液 发生氧化还原反应使之褪色 (化学方程式为。②根据图知,用氯化钠溶液电解得到naoh、氯气、氢气,氢氧化钠和二氧化硫反应生成亚硫酸钠和水,亚硫酸钠和稀盐酸反应生成氯化钠,能循环利用的物质是氯化钠,所以a为氢氧化钠,bc为氢气和氯气,两者反应生成d为氯化氢,c为亚硫酸钠,据此分析解答。d.碳碳不饱和键、醛基、连接苯环的碳原子上含有氢原子的苯的同系物都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色.。
 (催化剂:粉尘、五氧化二钒)
(催化剂:粉尘、五氧化二钒)
SO2+Cl2+2H2O=H2SO4+2HCl(将SO2气体和Cl2气体混合后作用于有色溶液,漂白效果将大大减弱。)
④SO2的弱氧化性:如2H2S+SO2=3S↓+2H2O(有黄色沉淀生成)
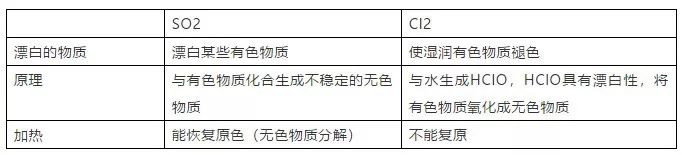
⑤SO2的漂白性:SO2能使品红溶液褪色,加热会恢复原来的颜色。用此可以检验SO2的存在。
⑥SO2的用途:漂白剂、杀菌消毒、生产硫酸等。
45、硫酸(H2SO4)
(1)浓硫酸的物理性质:纯的硫酸为无色油状粘稠液体,能与水以任意比互溶(稀释浓硫酸要规范操作:注酸入水且不断搅拌)。质量分数为98%(或18.4mol/l)的硫酸为浓硫酸。不挥发,沸点高,密度比水大。
(2)浓硫酸三大性质:吸水性、脱水性、强氧化性。
①吸水性:浓硫酸可吸收结晶水、湿存水和气体中的水蒸气,可作干燥剂,可干燥H2、O2、SO2、CO2等气体,但不可以用来干燥NH3、H2S、HBr、HI、C2H4五种气体。
②脱水性:能将有机物(蔗糖、棉花等)以水分子中H和O原子个数比2∶1脱水,炭化变黑。
③强氧化性:浓硫酸在加热条件下显示强氧化性(+6价硫体现了强氧化性),能与大多数金属反应,也能与非金属反应。
11. 1 二Ⅴa弱 2 1s22s22p63s23p4大3 cu+2h2so4 浓 cuso4+so2↑+2h2o考点集训1.c[a和b两个选项都是电子排布式,c和d两个选项都是轨道表示式,其中c选项违背了洪特规则。1.2h2so4(浓)+ cu =(加热)cuso4 + so2 + 2h2o2.h2so3 + 2naoh = na2so3 + 2h2o3.h2so3 + h2o2 = h2so4+ h2o4.h2s+x2(cl2,br2,i2)= s + 2hx5.h2s + h2o2 = s + 2h2o 6.h2s + na。
(此反应浓硫酸表现出酸性和强氧化性 )
b. 与非金属反应(如C反应):2H2SO4(浓)+C===△CO2 ↑+2H2O+SO2 ↑
(此反应浓硫酸表现出强氧化性 )
注意:常温下,Fe、Al遇浓H2SO4或浓HNO3发生钝化。
浓硫酸的强氧化性使许多金属能与它反应,但在常温下,铝和铁遇浓硫酸时,因表面被浓硫酸氧化成一层致密氧化膜,这层氧化膜阻止了酸与内层金属的进一步反应。这种现象叫金属的钝化。铝和铁也能被浓硝酸钝化,所以,常温下可以用铁制或铝制容器盛放浓硫酸和浓硝酸。
你怎么这样说话