国家不良反应检测中心 孙燕院士解读2018年ASCO临床肿瘤学进展(2)
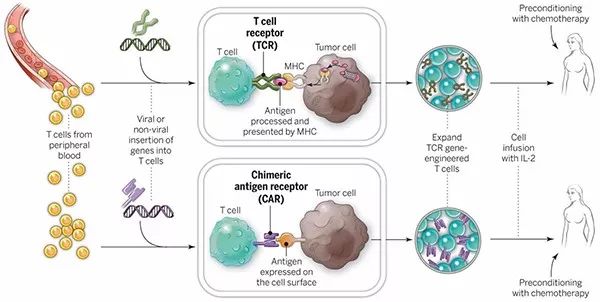
从2016年11月到2017年10月这一年间,美国FDA共批准了两个过继免疫疗法(adoptive immune therapy)。2017年8月,FDA批准了第一个CAR-T细胞疗法Tidagenlecleucel(商品名:Kymriah)用于治疗复发的青少年急性淋巴细胞白血病,结果80%的患者获得完全缓解,有的已经生存超过10年。
2017年10月,第二个CAR-T细胞疗法Axicabtagene ciloleucel(商品名:Yescarta),用于治疗B细胞淋巴瘤,也已经上市。
2. PD-L1/PD-1免疫检查点抑制剂
PD-L1/PD-1抑制剂已经有了比较广泛的研究。FDA已经批准其中4种进入临床。2017年Pembrolizumab(商品名:Kaytruda)成为第一个获批准的广谱免疫制剂。不论肿瘤在何部位,只需有特定基因变异——高微卫星不稳定性或错配修复缺陷(MSI-H或dMMR)这两项特征,就可以应用。这在很大程度上类似中医的“异病同治”。
另一个很有希望的新药物,Larotrectinib,针对一个罕见的肿瘤基因变异(TRK基因融合),也可以用于各种肿瘤类型。这个药物现在进行Ⅰ/Ⅱ期临床试验,如果通过FDA批准,就有望成为第一个“与肿瘤无关”的广谱靶向疗法。
三、靶向药物发展迅速且趋向成熟
+
2017年,美国FDA批准了13种新的靶向治疗,用于白血病、多发性骨髓瘤、卵巢癌、乳腺癌、肺癌。截至2017年,美国NCI的数据库中靶向药物已经涵盖了27种肿瘤。其中最多的是肺癌和淋巴瘤都是16种,其次是白血病15种、乳腺癌13种、肾癌11种、皮肤癌12种、黑色素瘤9种,其他分别为头颈部癌8种、多发性骨髓瘤7种、妇科肿瘤5种、大肠癌6种、消化系统癌5种、胰腺癌3种、胃癌2种、甲状腺癌4种、膀胱癌5种、肉瘤3种。说明在临床上超过半数患者在一定时期应考虑是否可以采用靶向药物。
NSCLC的靶向治疗第一代EGFR-TKI研究最多,临床应用的适应证也已经比较明确,有EGFR基因突变的患者无论早期或晚期都可以从中获益;耐药患者有T790M突变的患者接受第二代TKI奥希替尼(Osimertinib,AZD9291)治疗疗效明显,而且认识到具有ALK-EML4融合基因的患者也可能从PD-L1/PD-1抑制剂治疗中获益;第三代的TKI Olmutinib(奥姆替尼)疗效也比较肯定。具有ALK-EML4融合基因的患者应用克唑替尼的疗效突出,第二代的药物也进入临床试验。在临床上应用已经比较成熟,有效率可达60%~80%,而且不良反应少,在一定程度上在敏感患者可以取代化疗。

另外,特别令人鼓舞的是抗PD-L1/PD-1单抗与化疗联合应用。2017年5月Pembrolizumab(派姆单抗)联合化疗治疗非鳞NSCLC的结果,联合组有效率56.7%,而化疗组为31.7%;PFS分别是19.0个月和8.9个月。2017年12月,罗氏Atezolizumab+贝伐珠单抗+化疗治疗之前未接受过化疗的晚期非鳞NSCLC患者,有效率分别为65%和48%;PFS分别为8.3个月和6.8个月。2018年1月16日,默沙东宣布一项入组614例患者的Ⅲ期临床研究Keynote189研究,PD-1单抗联合化疗有效率和生存率较单用化疗均有较大幅度的提高。


《新英格兰医学杂志》(N Engl J Med)2018年2月21日在线发布,拜耳公司针对17种肿瘤的抗癌新药Larotrectinib(LOXO-101)的最新研究数据。Larotrectinib是第一个口服、针对存在NTRK1、NTRK2或NTRK3基因融合的乳腺癌、胆管癌、结直肠癌、胃肠道间质瘤(GIST)、婴儿纤维肉瘤、肺癌、黑色素瘤、胰腺癌、阑尾癌、甲状腺癌等17种肿瘤的高选择性TRK抑制剂,可用于年龄4个月至76岁的儿童和成人病人,抗肿瘤客观有效率高达75%,而且安全性好。这无疑是新春过后肿瘤治疗进展最振奋人心的重磅好消息。