衍生物 金属催化偶联反应小结(5)
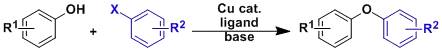
苯酚??醇类与卤代芳烃之间通过铜催化形成芳基醚的合成手法。
三十、,,
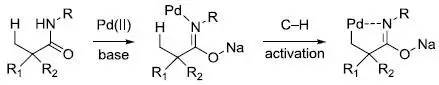
余金权及其课题组1,7发现一些位置选择性或立体选择性的C-H活化反应,此类反应的特点是利用钯催化并加入氧化剂,通常底物含有导向基团,另外加入一些优化的配体会增强选择性和加快反应速率。
经典的 sp2杂化C??H 活化:
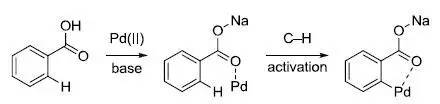
经典的 sp2杂化C??H 活化:
三十一、重氮偶联反应(diazocoupling)
重氮盐与富电子芳香环(苯胺,苯酚等)反应,得到偶氮化合物的反应,通常取代发生在对位。
三十二、脱羧偶联反应
脱羧偶联反应是指利用金属催化剂实现羧酸类化合物脱羧并在原来的羧酸位点生成新的碳-碳键的化学反应。广义上来说,也可以将金属催化羧酸脱羧并生成碳杂原子化学键(碳-氧,碳-硫,碳-氮键等)的反应归类为脱羧偶联反应。[1, 2, 3]传统有机化学中的脱羧反应主要利用了氧化羧酸生成自由基的过程。芳基和烯基(Csp2-COOH) 羧酸的脱羧偶联反应主要利用金属催化实现氧化还原中性条件下的脱羧,并且生成金属有机中间体,从而实现与亲电试剂或者在氧化性条件下与亲核试剂的偶联成键。虽然一些活化的烷基羧酸可以在金属催化剂催化下通过生成金属有机中间体的历程进行非自由基脱羧偶联。但是,针对金属催化剂催化烷基羧酸(Csp3-COOH)的脱羧困难问题,一些烷基羧酸的脱羧偶联反应仍然需要通过自由基反应机理进行。值得指出的是,最近,MacMillan等人成功将光氧化还原催化剂与镍催化剂结合,通过结合光催化与金属有机催化的混合手段,实现了氨基酸和非活化烷基羧酸的脱羧偶联。
三十三、芳香卤代烃在金属催化作用下的腈化反应
芳腈化合物在有机合成中占据非常重要的地位,尤其是在染料,除草剂,农用化学品,药物及自然产品中应用非常广泛。传统方法合成芳腈化合物主要通过苯胺的重氮化接着Sandmeyer反应制得,对不是复杂的苯腈可由甲苯类化合物在NH3作用下直接氧化制备。但这些方法有较大局限性:反应条件较剧烈,底物要比较简单取代基较少,毒性很大。以下介绍的是实验室常用方法。
三十四、常见钯催化剂的制备
在有机合成中常见的钯催化偶联反应有:Suzuki-Miyaura偶联, Stille偶联, Negishi偶联, Kumada偶联, Hiyama偶联, Sonogashira偶联, Heck反应, Buchwald-Hartwig反应等等。因此常见的钯催化剂应用非常广泛,虽然这些催化剂都已商业化,但对于大规模生产的反应,可以自己制备降低成本。
三十五、Liebeskind偶联反应
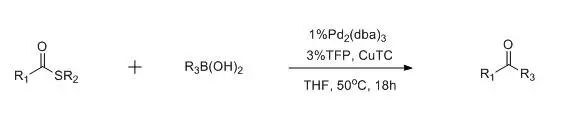
2000年Libeskind和Srogl提出了一种在中性条件下,过渡金属催化硫酯和硼酸进行偶联得到酮的新方法。在化学计量的噻吩-2-羧酸亚铜(CuTC)和催化量的钯催化下,硫代酸酯和芳基硼酸或烷基硼进行偶联得到酮的反应被称为Libeskind偶联反应。此反应是非常重要的把羧酸及其衍生物转化为酮的方法,此反应中硼酸或烷基硼为非碱性亲核试剂,因此反应条件比Fuyama偶联更温和。
三十六、Reformatsky反应
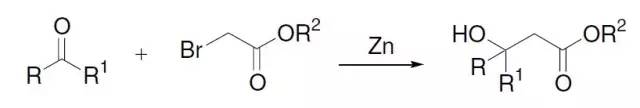
由α-卤代酯和锌粉制备得到的有机锌试剂对羰基化合物(醛、酮、酯)进行亲核加成生成β-羟基酯的反应。
不同的α-卤代酯的活性次序为:碘代酸酯>溴代酸酯>氯代酸酯>氟代酸酯,因氟和氯代酯不活泼,而碘代酯较难制备,故常用溴代酸酯。反应溶剂常用绝对无水有机溶剂,最常用的有乙醚、苯、甲苯、二甲苯等。
α-卤代酯不能与镁反应生成格氏试剂,但易与锌形成有机锌化合物。这是制备β-羟基酯的一个很好的方法。β-羟基酯可以用于制备β-羟基酸和α,β-不饱和酯。
有机锌试剂的活性比格氏试剂低,因此此反应的官能团兼容性高,但反应较慢。近年来,也有发现除锌以外的金属也能发生类似的反应,特别是Sm(II)、Cr(II)、Ti(II),B(III)等。
三十七、Roskamp-Feng反应
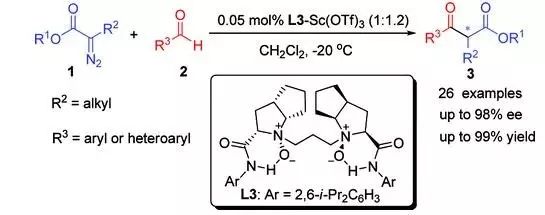
1989年,Roskamp首先报道了利用氯化亚锡催化乙基重氮乙酸乙酯和醛反应制备β-酮酯的反应【J. Org. Chem.,1989, 54, 3258】。经过二十多年的发展各种路易斯酸(Sc(OTf)3,BF3, GeCl2)都可用于此反应。2011年,四川大学化学学院冯小明教授,以手性氮氧–Sc(OTf)3络合物催化剂实现了首例催化不对称Roskamp反应。