化学实验室制取氧气的反应原理及仪器、装置的探讨
氧气的 制取一、教学目标: 知识与技能: 了解实验室制取氢气的主要方式跟原理,初步知道借助物理试验制取氢气的方式。 过程与技巧: 1.能够按照反应物的性质跟反应条件来选取制备氢气的试验装置与操作方法,会据生成 物的性质选择收集方式。 2.学会边实验、边讨论、边研究的方式,在活动中唤起学习兴趣,在兴趣中强调问题、分 析问题、解决难题。 情感态度与价值观: 1.学生从中养成实事求是,严肃认真的科学态度跟良好的实验习惯。 2.保持对物理实验的独特兴趣,从而促使教师学习化学的自觉性和积极性。 二、教学重点: 1.实验室制取氢气的反应机理。 2.实验室制取氢气的发生装置及收集装置的阐述。 三、教学难点: 实验室制取氢气的反应机理及设备、装置的阐述。教学过程 一、 实验室制法 1、高锰酸钾制取氢气 加热 a. 实验原理:高锰酸钾——→ 锰酸钾+ 二氧化锰+氧气 KMnO4 b.实验装置 K2MnO4 MnO2 O2教学拓展发生装置收集装置c. 实验方法: a).查:将导管的一端浸入水槽中,用手握住试管外壁,若水中的导管口有 气泡冒出,证明装置不生锈。松开手后,导管口发生一段水柱。 b). 装:按粉末状固体取用的方式(药匙或纸槽)。
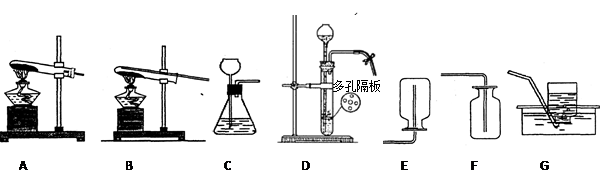
c). 定:先下后上,从左至右的排序。 先让试管均匀受热,后在反应物部位用酒精灯外焰由前向后加热。 d). 点: e). 收:若用排水集气法收集氢气教案模板化学氧气,当气泡均匀冒出时再收集;或向上集 气法。 f). 离:移离导气管。g). 熄:熄灭酒精灯 注意事项: d. a). 试管口应略微向下倾斜:防止生成的水回流,使试管底部破裂。 b). 导气管伸入发生装置内应稍露出橡皮塞:有利于产生的氨气排出。 c). 试管口塞一团棉花:防止高锰酸钾粉末进入导气管,污染制取的氨气 和水箱中的水。 d). 排气法收集氧气时,导气管要伸入接近集气瓶底部:有利于集气瓶内 空气排出,使收集的氧气最纯。 e). 实验结束后,先将导气管移出水面,然后点燃酒精灯:防止水槽中的 水倒流,炸裂试管。 2、双氧水(过氧化氢)制取氢气 a. 实验原理: 二氧化锰 过氧化氢(H2O2) ————→ 水(H2O) + 氧气(O2) b. 注意事项: a). 分液漏斗可以用长颈漏斗代替,但其上方应该深入液面以下,防止生 成的氨气从长颈漏斗中逸出; b). 导管只需略微伸入试管塞 c). 气密性检查:用止水夹关闭,打开分液漏斗活塞,向漏斗中加入水, 水面不大幅增加,就表明气密性良好。
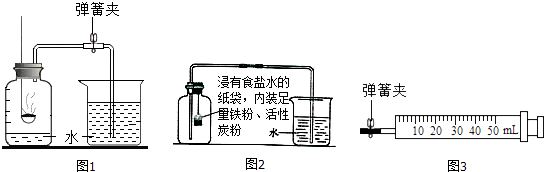
d). 装药品时,先装固体后装液体 e). 该装置的特点:可以控制反应的起初与结束,可以随时添加液体。 总结:若固体(或液态+固体)加热生成氢气,选用高锰酸钾制氯气装置; 若液态+液体常温下制备氢气,选用三乙胺制取氮气装置。 催化剂: 在化学反应中可改变其它物质的反应速度, 但原本的化学性质和质 量在反应前后没有发生差异的物质。 二、工业制法(分离液态空气法) (1)具体过程 空气除去二氧化硫 干燥气体降温-196℃ 升温-183℃空气降温 加压液态空气液态氧氧气(2)注意:该过程是物理变化 补充练习测试题: (1)从液体空气分离气体和氢气,为什么得到的是气态氢跟液体氧? (2)用氧炔焰焊接和切割金属时,发生三种差异:乙炔在气体中燃烧;焊 接处塑料与金属焊剂熔化、 冷却后凝结在一起; 切割处的塑料在高温下被氧 气氧化除去。这三种差异哪些是物理变化?哪些是物理差异? (3)从液体空气、高锰酸钾、双氧水三种物质制氯气时,各物质出现的是 物理变化还是物理差异?为什么? (4)空气中有气体,带余烬的钢条塞进装有空气的集气瓶教案模板化学氧气,木条是否会复 燃?为什么? 反思:实验最有趣,但学生在实验后仍然收获很少,以后教学中可以先讲后 做,再讲,最后借助学生实验进行巩固。

盯住日本动态