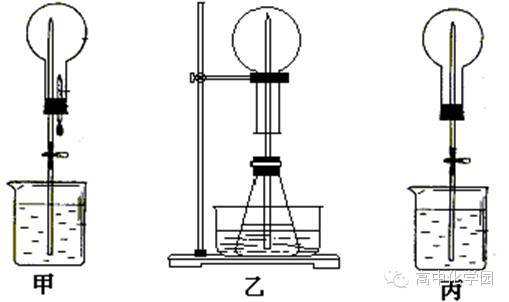
右图是实验室进行氨溶于水的喷泉实验装置,下列叙述不正确的是(

磷在自然界中的存在:
自然界中没有游离态的磷,磷主要以磷酸盐的形式存在于矿石中。磷和氮一样,是构成蛋白质的成分之一。动物的骨骼、牙齿和神经组织,植物的果实和幼芽,生物的细胞里都含有磷,磷对维持生物体正常的生理机能起着重要的作用。
磷的物理性质:
磷的单质有多种同素异形体,其中常见的是白磷和红磷。白磷和红磷的主要性质如下表。

特别提醒白磷遇光会逐渐变为黄色。因此,白磷又称黄磷,白磷的颜色往往表述为“白色或黄色”。
白磷和红磷的化学性质:
利用白磷燃烧消耗空气中的氧气生成白色固体五氧化二磷,而使试管内气体体积减小,测出气体减少的体积即为试管内空气中所含氧气的体积。6. 红磷在空气中燃烧(研究空气组成的实验):4p + 5o2 =点燃= 2p2o5。(2)为验证空气中氧气的含量,小雅同学选用40ml的试管和量程足够大且润滑效果很好的注射器等作器材(如上图).将足量的比红磷更易燃烧的白磷放入试管,用橡皮塞塞紧管口,夹紧弹簧夹.点燃酒精灯,使白磷在试管中燃烧(产物为五氧化二磷),燃烧结束待试管冷却后松开弹簧夹,观察现象.。
磷的用途:
白磷和红磷有许多用途,如都可用于制造纯度较高的磷酸;白磷可用于制造燃烧弹、烟幕弹等;红磷可用于制农药、安全火柴等。
白磷和红磷的分子结构:
4.氨气分子空间构型是三角锥形,而甲烷分子是正四面体,这是因为()a.两种分子的中心原子的杂化轨道类型不同,nh3为sp2型杂化,而ch4是sp3型杂化b.nh3分子中氮原子形成3个杂化轨道,ch4分子中碳原子形成4个杂化轨道c.nh3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强d.氨气分子是极性分子而甲烷是非极性分子解析:选cnh3和ch4的中心原子都是sp3杂化,故a、b错误。 题型构建c ( ) 题组一判断烃的空间结构1. 下列关于甲烷结构的说法中正确的是a. 甲烷的分子式是 ch4 , 5 个原子共面 b. 甲烷分子中, 碳原子和氢原子形成了 4 个不完全相同的碳氢共价键 c. 甲烷分子的空间构型属于正四面体结构 d. 甲烷中的任意三个原子都不共面 解析 甲烷分子中的 5 个原子最多 3 个原子共面, 选项 a、 d 错。判断abn型分子是否有极性,关键是看分子的立体构型.如果分子的立体构型为直线形、平面三角形、正四面体形、三角双锥形、正八面体形等空间对称的结构,致使正电中心与负电中心重合,这样的分子就是非极性分子。

特别提醒白磷和红磷的化学式通常都写为P。
磷的化合物:
(1)五氧化二磷:
五氧化二磷的分子式为 ,通常写为
,通常写为 ,
, 分子的空间构型如图所示。
分子的空间构型如图所示。

五氧化二磷通常为白色固体,由磷在空气中燃烧生成, 632K时升华。
五氧化二磷是典型的酸性氧化物,具有酸性氧化物的通性。
五氧化二磷很易跟水反应,跟冷水反应生成偏磷酸,跟热水反应生成磷酸,反应放出大量的热。

五氧化二磷的强亲水性决定了它可用作干燥剂。五氧化二磷是一种固态、酸性、无强氧化性的干燥剂,干燥能力非常强。
(2)磷酸:
磷酸为三元中强酸,属于弱电解质,易溶于水,在水中分三级电离。高中化学喷泉实验

纯磷酸是无色晶体,熔点为315K.沸点较高,可溶于水。
具有酸的通性 磷酸三步电离常数与碱反应 naoh+h3po4=nah2po4+h2o 2naoh+h3po4=na2hpo4+2h2o 3naoh+h3po4=na3po4+3h2o 与某些盐反应 nabr+h3po4 =nah2po4+hbr↑ nai+h3po4= nah2po4+hi↑ 原理:难挥发性酸制挥发性酸 磷酸根离子具有很强的配合能力。 15、氢溴碘酸真刁难,不用硫酸用磷酸:意思是说制备氢溴酸和氢碘酸时,不能用浓硫酸,而必须用磷酸,反应式为:nabr +h3po4 = hbr↑ + nah2po4 ,nai + h3po4 = hi↑ + nah2po4[联想:因为浓硫酸具有强氧化性,可把生成的hbr和hi氧化br2和i2,反应式为:2hbr +h2so4 = so2↑+ br2 + 2h2o ,2hi + h2so4 = so2↑ +i2 +2h2o]。1氢溴碘酸真刁难,不用硫酸用磷酸:意思是说制备氢溴酸和氢碘酸时,不能用,而必须用磷酸,反应式为:nabr+h3po4=hbr↑+nah2po4,nai+h3po4=hi↑+nah2po4[联想:因为具有强氧化性,可把生成的hbr和hi氧化br2和i2,反应式为:2hbr+h2so4=so2↑+br2+2h2o,2hi+h2so4=so2↑+i2+2h2o]。
(3)磷酸盐:
磷酸是三元酸,对应的盐有正盐和酸式盐:  .
.
氮气的物理性质和化学性质:
28,四个氢原子无色、 无味的气体, 密度比空气小, 极难溶于水二、 甲烷的性质1 物理性质1 6向下排空气法排水法甲烷甲烷2、 甲烷的化学性质通常情况下, 甲烷的结构比较稳定, 不易与其它物质反应。1、物理性质:无色,无味的气体,密度比空气大,能溶于水,高压低温下可得固体----干冰。物理性质 无色、无味、难溶于水、密度比空气小的气体,是天然气、沼气、油田气、煤道坑气的主要成分 无色、稍有气味的气体,难溶于水,密度略小于空气 无色、有特殊香味的液体,不溶于水,密度比水小,有毒。
二氧化硫中硫元素的化合价为+4价,是硫元素的中间价态,所以so2既有氧化性又有还原性,选c。原子或离子化合价升高总数=原子或离子化合价降低总数。d.由于单质cl2中元素的化合价在cl元素之间,既可以升高,也可以降低。
①N2与H2化合生成NH3:
说明:该反应是一个可逆反应,是工业合成氨的原理。
②N2与金属反应(Mg Ca Sr Ba)反应:
③N2与O2化合生成NO:
说明:在闪电或行驶的汽车引擎中会发生以上反应。
氮气的用途:
①合成氨,制硝酸;
②代替稀有气体作焊接金属时的保护气,以防止金属被空气氧化;
⑧在灯泡中填充氮气以防止钨丝被氧化或挥发;

④保存粮食、水果等食品,以防止腐烂;
⑤医学上用液氮作冷冻剂,以便在冷冻麻醉下进行手术;
⑥利用液氮制造低温环境,使某些超导材料获得超导性能。
二氧化氮的物理性质和化学性质:
(1)物理性质:红棕色、有刺激性气味、有毒的气体,易溶于水、易液化,比空气重。
(2)化学性质:
与H2O反应: 
(工业制HNO3原理,在此反应中,NO2同时作氧化剂和还原剂)
隐含反应: 的应用:
的应用:
通常“纯净”的NO2或N2O4并不纯,因为在常温、常压下能发生反应 ,由于此平衡的存在,导致一些物理量的理论值与实验值有一定的误差。高中化学喷泉实验例如:
,由于此平衡的存在,导致一些物理量的理论值与实验值有一定的误差。高中化学喷泉实验例如:
1.收集到的1mo1NO2在标准状况下的体积应小于22.4L
2.标准状况下22.4LNO2的质量大于46g。
3.NO与O2混合后,所得物质的相对分子质量应大于按体积比求得的数值。
4.温度影响“ ”平衡体系,其他条件不变,体系颜色随温度改变而改变。升高温度,气体颜色变深;降低温度,气体颜色变浅。
”平衡体系,其他条件不变,体系颜色随温度改变而改变。升高温度,气体颜色变深;降低温度,气体颜色变浅。

5.恒容时,在“ ”平衡体系中增加 N01,相当于增大压强。
”平衡体系中增加 N01,相当于增大压强。
有关混合气体NO、NO2、O2溶于水的计算:

①×2+②得NO2、O2与水反应生成HN3,的化学方程式为:

①×2+②×3得NO、O2与水反应生成HNO3的化学方程式为:

一般NO、NO2、O2与水反应,可归纳成四种情况:
1.NO和NO2混合
 剩余气体为NO
剩余气体为NO
2.NO2和O2混合

3.NO和O2混合

4.NO2、NO、O2的混合
当 时,反应后无气体剩余
时,反应后无气体剩余
12、气瓶中的气体不得全部用完,氧气瓶内的剩余压力不小于0.147mpa(1.5kg/cm2),。剩余几种情形都是一般情形的特例。最后将会吹散掉剩余在行星盘的气体。
今天股票军工股长势喜人