有机物的性质及鉴别总结完整版

苯并(a)芘的结构简式如图所示,下列有关苯并(a)芘的说法中不正确的是( ) a. 苯并(a)芘的分子式为 c20h12, 属于稠环芳香烃 b. 苯并(a)芘与互为同分异构体 c. 苯并(a)芘在一定条件下可以发生取代反应, 但不能使酸性 kmno4溶液褪色 d. 苯并(a)芘不易溶于水, 易溶于苯、 氯仿等有机溶剂 知识梳理·。7.(2017·湖北4月调研)下列关于有机物的叙述正确的是()a.乙烯和苯都能使溴水褪色,褪色的原因相同b.分子式为c2h4o2且能与naoh溶液反应的有机物一定是乙酸c.油脂和纤维素都是能发生水解反应的高分子化合物d.甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应答案d解析乙烯结构简式为ch2===ch2,含有碳碳双键,和溴水发生加成反应,苯使溴水褪色,利用溴单质易溶于有机溶剂,属于萃取,因此原理不同,a项错误。d.碳碳不饱和键、醛基、连接苯环的碳原子上含有氢原子的苯的同系物都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色.。
立刻饮服下列溶液,使其生成草酸钙沉淀:1、在200毫升水中,溶解30克丁酸钙或其它钙盐制成的溶液2、大量牛奶,可饮食用牛奶打溶的蛋白作镇痛剂。稳定性:在通常贮存的条件下稳定.溶于丙酮和甲醇,那么应该溶于大部分的有机溶剂,你可以试试异辛酸(228℃) ,或者是硝基乙烷 114.0 辛烷 125.67 几乎不溶于水,微溶于乙醇,与醚、丙酮、石油醚、苯、氯仿、汽油混溶乙酸丁酯 126.11 优良有机溶剂,广泛应用于医药行业,还可以用做萃取剂氯苯 131.69 能与醇、醚、脂肪烃、芳香烃、和有机氯化物等多种有机溶剂混溶对二甲苯 138.35 不溶于水,与醇、醚和其他有机溶剂混溶二甲苯 138.141.5 不溶于水,与乙醇、乙醚、苯、烃等有机溶剂混溶,乙二醇、甲醇、2-氯乙醇等极性溶剂部分溶解间二甲苯 139.10 不溶于水,与醇、醚、氯仿混溶,室温下溶解乙睛、dmf等醋酸酐 140.0 邻二甲苯 144.41 不溶于水,与乙醇、乙醚、氯仿等混溶环己酮 155.65 与甲醇、乙醇、苯、丙酮、己烷、乙醚、硝基苯、石油脑、二甲苯、乙二醇、乙酸异戊酯、二乙胺及其他多种有机溶剂混溶糠醛 161.8 与醇、醚、氯仿、丙酮、苯等混溶,部分溶解低沸点脂肪烃,无机物一般不溶邻甲酚 190.95 微溶于水,能与乙醇、乙醚、苯、氯仿、乙二醇、甘油等混溶n,n-二甲基苯胺 193 微溶于水,能随水蒸气挥发,与醇、醚、氯仿、苯等混溶,能溶解多种有机物对甲酚 201.88 n-甲基吡咯烷酮 202 硝基苯 210.9 喹啉 237.10 乙二醇碳酸酯 238 二甘醇 244.8。是不是这个实验啊1、取1支试管,加入1ml卵蛋清溶液,再加入2%硫酸铜溶液1滴,观察沉淀生成.2、再向试管中加入过量的饱和硫酸铜溶液,观察沉淀的溶解.盐溶液(比如硫酸铜)使蛋白质沉淀的原因不是蛋白质变性而是盐析,少量的盐溶液改变了蛋白质的溶解度,所以在步骤一的时候,溶剂(水)的量相对不足,所以发生了沉淀,但是当加入足够。
na2co3溶液的作用是:⑴饱和碳酸钠溶液的作用是冷凝酯蒸气。油脂的皂化是酯类的碱性水解,油脂是高级脂肪酸和甘油(丙三醇)形成的酯,不属于高分子,所以油脂皂化不是高分子生成小分子的过程,d项错误。③乙烯基树脂中,每单位相对分子质量中的酯键比普通不饱和聚酯中少35%~50%左右、耐热性和耐腐蚀性能,经过交联单体或活性溶剂稀释形成的具有一定黏度的树脂溶液,分子链中易被水解遭受破坏的酯键间的间距增大,常压下成型一般是由不饱和二元酸二元醇或者饱和二元酸不饱和二元醇缩聚而成的具有酯键和不饱和双键的线型高分子化合物、稀酸、稀碱的性能较好,耐有机溶剂的性能差,同时。
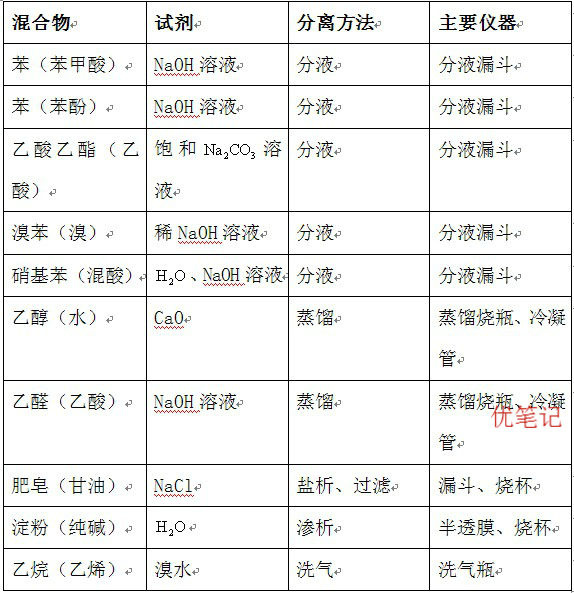
☆ 一卤代烷不愉快的气味, 有毒, 应尽量避免吸入。 ☆ C4以下的一元醇有酒味的流动液体 ☆ C5~C11的一元醇 ☆ C12以上的一元醇 ☆ 乙醇 ☆ 乙二醇 ☆ 丙三醇(甘油) ☆ 乙醛 ☆ 乙酸不愉快气味的油状液体 无嗅无味的蜡状固体特殊香味 甜味(无色黏稠液体) 甜味(无色黏稠液体) 刺激性气味 强烈刺激性气味(酸味)☆ 低级酯 二、 重要的反应 1. 能使溴水(Br2/H2O) 褪色的物质芳香气味 (1) 有机物 通过加成反应使之褪色: 含有、 —C≡C—的不饱和化合物 通过氧化反应使之褪色: 含有—CHO(醛基) 的有机物 通过萃取使之褪色: 液态烷烃、 环烷烃、 苯及其同系物、 饱和卤代烃、 饱和酯 (2) 无机物 ① 通过与碱发生歧化反应 3Br2 + 6OH- == 5Br- + BrO3- + 3H2O 或 Br2 + 2OH- == Br- + BrO2-、 I- + H2O -、 Fe② 与还原性物质发生氧化还原反应, 如 H2S、 S2. 能使酸性高锰酸钾溶液 KMnO4/H+褪色的物质 2-、 SO2、 SO32+ (1) 有机物: 含有、 —C≡C—、 —CHO 的物质 与苯环相连的侧链碳碳上有氢原子的苯的同系物(与苯不反应) (2) 无机物: 与还原性物质发生氧化还原反应, 如 H2S、 S2-、 SO2、 SO32-、 Br-、 I-、 Fe2+ 3. 与 Na 反应的有机物: 含有—OH、 —COOH 的有机物 与 NaOH 反应的有机物: 常温下, 易与含有酚羟基. . .、 —COOH 的有机物反应 加热时, 能与酯反应(取代反应) 与 Na2CO3反应的有机物: 含有酚.羟基的有机物反应生成酚钠和 NaHCO3; 含有—COOH 的有机物反应生成羧酸钠, 并放出 CO2气体; 与 NaHCO3反应的有机物: 含有—COOH 的有机物反应生成羧酸钠并放出等物质的量的 CO2气体。
4.加碱可使乙醛与银氨溶液在常温下发生反应,但如果滴加氢氧化钠过量,反应速率太快,产生的银镜会发黑。故要先把甲酸用氢氧化钠溶液中和,然后再与银氨溶液反应。19.检验蔗糖、淀粉、纤维素是否水解时,先在水解后的溶液中加naoh溶液中和h2so4,再加银氨溶液或cu(oh)2悬浊液。
(2) 斐林试剂的配制: 向一定量 10%的 NaOH 溶液中, 滴加几滴 2%的 CuSO4溶液, 得到蓝色絮状悬浊液(即斐林试剂) 。 (3) 反应条件: 碱过量、 加热煮沸. . . . . . . . (4) 实验现象: ① 若有机物只有官能团醛基(—CHO) , 则滴入新制的氢氧化铜悬浊液中, 常温时无变化, 加热煮沸后有(砖)红色沉淀生成; ② 若有机物为多羟基醛(如葡萄糖) , 则滴入新制的氢氧化铜悬浊液中, 常温时溶解变成绛蓝色溶液, 加热煮沸后有(砖) 红色沉淀生成; (5) 有关反应方程式: 2NaOH + CuSO4 == Cu(OH)2↓ + Na2SO4RCHO + 2Cu(OH)2RCOOH + Cu2O↓+ 2H2OHCHO + 4Cu(OH)2CO2 + 2Cu2O↓+ 5H2OOHC-CHO + 4Cu(OH)2HOOC-COOH + 2Cu2O↓+ 4H2OHCOOH + 2Cu(OH)2CO2 + Cu2O↓+ 3H2O CH2OH(CHOH)4CHO + 2Cu(OH)2CH2OH(CHOH)4COOH + Cu2O↓+ 2H2O (6) 定量关系: —COOH~½ Cu(OH)2~½ Cu2+ (酸使不溶性的碱溶解) —CHO~2Cu(OH)2~Cu2O 6. 能发生水解反应的有机物是: 酯、 糖类(单糖除外) 、 肽类(包括蛋白质) 。
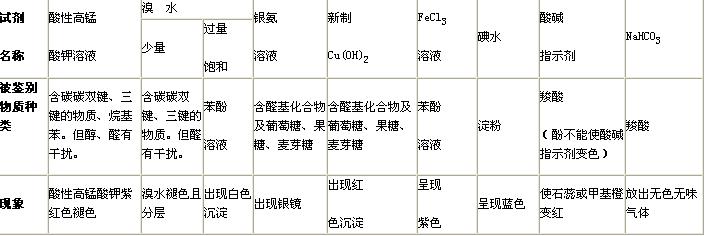
HCHO~4Cu(OH)2~2Cu2OHX + NaOH == NaX + H2O(H)RCOOH + NaOH == (H)RCOONa + H2ORCOOH + NaOH == RCOONa + H2O 或 7. 能跟 I2发生显色反应的是: 淀粉。 8. 能跟浓硝酸发生颜色反应的是: 含苯环的天然蛋白质。 三、 各类烃的代表物的结构、 特性 类 别 烷 烃 烯 烃 炔 烃 苯及同系物 通 式 CnH2n+2(n≥1) CnH2n(n≥2) CnH2n-2(n≥2) CnH2n-6(n≥6) 代表物结构式 H—C≡C—H 相对分子质量Mr 16 28 26 78 碳碳键长1.54 1.33 1.20 1.40 (×10-10m) 键 角 109°28′ 约 120° 180° 120° 分子形状 正四面体 6 个原子 共平面型 4 个原子 同一直线型 12 个原子共平面(正六边形) 主要化学性质 光 照 下 的 卤代; 裂化; 不使酸性 KMnO4溶液褪色 跟 X2、 H2、 HX、H2O、 HCN 加成,易被氧化; 可加聚 跟 X2、 H2、 HX、HCN 加成; 易被氧化; 能加聚得导电塑料 跟 H2 加 成;FeX3催化下卤代;硝化、 磺化反应 四、 烃的衍生物的重要类别和各类衍生物的重要化学性质 类别 通 式 官能团 代表物 分子结构结点 主要化学性质 醇 一元醇: R—OH 饱 和 多 元醇: CnH2n+2Om 醇羟基 —OH CH3OH (Mr: 32) C2H5OH (Mr: 46) 羟基直接与链烃基结合, O—H 及C—O 均有极性。
油化工发展水平,所以a是h2c=ch2,e是具有果香味的有机物,e是酯,酸和醇反应生成酯,则b和d一种是酸一种是醇,b能被氧化生成c,a反应生成b,碳原子个数不变,所以b是乙醇,d是乙酸,铜作催化剂、加热条件下,乙醇被氧气氧化生成c,所以c是乙醛,a反应生成f,f是一种高聚物,可制成多种包装材料,所以f是聚乙烯,则。7.根据权利要求i所述提高草酸酯催化加氢制こニ醇选择性的方法,其特征在于在氢/酷摩尔比为100 150 : i的条件下使原料与催化剂接触反应o. i 150小时,之后将氢/酯摩尔比降至60 100 i继续进行反应。(7)乙烯和水在催化剂作用下加成生成乙醇,乙醇氧化生成乙醛,乙醛在题给信息的条件下反应生成,在浓硫酸加热条件下发生消去反应生成chcho在催化剂、氧气加热条件下发生催化氧化生成和乙醇发生酯化反应,即可得物质e,合成路线为:答案 (1)(2)浓hno3和浓h2so4(3) (4)碳碳双键、酯基(5)加聚反应(6) +nc2h5oh原创总结有机合成路线设计思维导图(2016·江苏,20(5))化合物h是合成抗心律失常药物的一种中间体,可通过以下方法合成:已知:1.苯胺易被氧化请以甲苯和(ch3co)2o为原料制备,写出制备的合成路线流程图(无机试剂任用)。
ru(oh)4的沉淀物用3l6mhcl溶液溶解,用稀碱调节至ph为1左右加入蒸馏釜中,连接好钌的吸收系统,蒸馏釜升温至80℃,逐渐向其中加入20%的naoh溶液和20%的nabro3溶液,当检查到有ruo4气体逸出时,停止加naoh溶液而继续加入nabro3溶液,继续蒸馏,直至检验无ruo4气体,蒸馏共持续12h。提取冶金中利用锇、钌易氧化为强挥发性的八价氧化物的性质与其他金属分离,然后用冷态的稀碱溶液和稀盐酸溶液分别吸收,相互分离。沉淀出的ru(oh)4用盐酸溶解,浓缩并用稀碱液调节至ph为1左右,加入蒸馏釜,逐渐升温至50~90℃,缓慢地加入20%naoh溶液和20%溴酸钠溶液,待有ruo4气体逸出后,停止加入氢氧化钠溶液,继续加入溴酸钠溶液直到无ruo4气体为止。

因此, 具有相同通式的有机物除烷烃外都不能确定是不是同系物。 此外, 要熟悉习惯命名的有机物的组成,如油酸、 亚油酸、 软脂酸、 谷氨酸等, 以便于辨认他们的同系物。 ( 二) 、 同分异构体的种类 常见的类别异构 组成通式 可能的类别 典型实例 CnH2n 烯烃、 环烷烃 CH2=CHCH3与 CnH2n-2 炔烃、 二烯烃 CH≡C—CH2CH3与 CH2=CHCH=CH2 CnH2n+2O 饱和一元醇、 醚 C2H5OH 与 CH3OCH3 CnH2nO 醛、 酮、 烯醇、 环醚、 环醇 CH3CH2CHO、 CH3COCH3、 CH=CHCH2OH 与 CnH2nO2 羧酸、 酯、 羟基醛 CH3COOH、 HCOOCH3与 HO—CH3—CHO CnH2n-6O 酚、 芳香醇、 芳香醚 与 CnH2n+1NO2 硝基烷、 氨基酸 CH3CH2—NO2与 H2NCH2—COOH Cn(H2O)m 单糖或二糖 葡萄糖与果糖(C6H12O6)、 蔗糖与麦芽糖(C12H22O11) ( 三) 、 同 分异构体的书写规律 书写时, 要尽量把主链写直, 不要写得扭七歪八的, 以免干扰自己的视觉; 思维一定要有序, 可按下列顺序考虑: 1. 主链由长到短, 支链由整到散, 位置由心到边, 排列邻、 间、 对。
帮做不断提高产品质量