关于化学反应与能量的说法_化学能量变化图怎么看_化学原电池反应

一、单选题(每小题只有一个正确答案)
1.在测定中和热的实验中,使用下列用品不是为了减小实验误差的是()*
2.下列关于反应热的表述正确的是( )*
3.物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是()
*
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________。解:由甲醇燃烧生成和液态水时放热,则甲醇燃烧放出的热量为,即燃烧热,。下列做法有利于生态环境保护的是a.焚烧落叶,减少垃圾的运输量b.大力植树造林,增加植被面积c.为增加节日气氛大量燃放烟花爆竹 d.大量使用农药和化肥,增加农作物产量2.下列变化属于化学变化的是a.冰雪融化b.分离液态空气制氧气c.石蜡熔化d.酒精燃烧3.下列化学仪器对应的名称书写正确的是a.长劲漏斗b.量桶c.坩埚钳d.椎形瓶4.下列有关实验现象的描述中,正确的是a.加热试管内的碱式碳酸铜,绿色粉末逐渐变黑,试管口有小水滴b.细铁丝在氧气中燃烧,火星四射,生成红棕色固体c.镁条在空气中燃烧,产生黑烟,生成黑色粉末d.红磷在空气中燃烧产生大量白色烟雾5.溶液的知识广泛用于生产、生活。
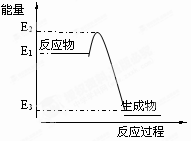
6.反应A+B→C分两步进行:①A+B→X,②X→C,反应过程中能量变化如图所示关于化学反应与能量的说法,E1表示反应A+B→X的活化能。下列有关叙述正确的是 ()
*
7.已知25 ℃、101 kPa时,乙烯和乙炔(C2H2)燃烧的热化学方程式分别为C2H4(g)+3O2(g)===2CO2(g)+2H2O(l)ΔH=-1411 kJ·mol-1,2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)ΔH=-2600 kJ·mol-1,又知燃烧时火焰的温度乙炔高于乙烯。据此,下列说法不正确的是()*
8.已知下列反应的反应热:

①CH3COOH(l)+2O2(g)====2CO2(g)+2H2O(l)ΔH1=﹣870.3 kJ·
③ C(s)+O2(g)====CO2(g)ΔH2=﹣393.5 kJ·
④ H2(g)+O2(g)====H2O(l)ΔH3=﹣285.8 kJ·
则2C(s)+2H2(g)+O2(g)====CH3COOH(l)的反应热为()*
9.下列有关反应能量变化图像的判断错误的是()

*
10. 已知H+(aq)+OH-(aq)===H2O(l)ΔH=-57.3 kJ·mol-1,下列反应放热为57.3 kJ的是()*
例如,测定 298 k 时 cl- 的标准摩尔生成焓时,先测定出下列反应的标准摩尔焓变 : 反应的标准摩尔焓变为: 例 1-4 计算下列反应在 298 k 的标准摩尔焓变: 解:由附录二查得: 298 k 时反应的标准摩尔焓变为: b 的燃烧反应的通式为: 定义温度 t 时 b 的燃烧反应的标准摩尔焓变为 b 的标准摩尔燃烧焓,用符号 表示。(3)已知pcl3是不稳定的无色液体,遇水反应可生成两种酸,该反应的化学方程式 为,所得含氧酸(已知该含氧酸的各步电离平衡常数分别为ka1=1.6×10﹣2和ka2=7×10﹣7)和足量的naoh溶液反应生成盐的化学式为.。已知α-氨基丙酸的结构简式为,它可与naoh反应生成α-氨基丙酸钠,其化学式为c3h6o2nna,又知味精的主要成分是谷氨酸一钠,它可以由谷氨酸与与naoh反应生成关于化学反应与能量的说法,其结构简式为,。
12.下列热化学方程式中ΔH表示可燃物燃烧热的是()*
13.下列说法或表示法正确的是()*

14.现有下列热化学方程式:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566 kJ·mol-1
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH3=-890 kJ·mol-1
④CH3CH2OH(l)+3O2(g)===2CO2(g)+3H2O(l) ΔH4=-1367 kJ·mol-1
下列说法不正确的是()*
而在异面过程中,生成键或断裂键处于反应体系的相反方面(图5)。(3)明确:旧键的断裂和新键的生成必须通过反应物分子(或离子)的相互接触、碰撞来实现。d、氯化氢溶于水,只存在旧键的断裂,没有新键生成,故d错误。
加油