高中常见气体的实验室和工业制法 请分开写 最好有装置图片
1.氢气
(1)工业制法:
①水煤气法:(高温条件下还原水蒸气)
单质+化合物化合物+单质: C+H2O(g) = CO+H2 ;
化合物+化合物化合物+单质:CO+ H2O(g) =CO2+H2
②氯碱工业的副产物:(电解饱和食盐水)
溶液A+B+C :2NaCl+2H2O=NaOH +H2↑+ Cl2↑,
(2)实验室制法:
①金属与非氧化性强酸的置换反应:
单质+化合物化合物+单质:Zn+H2SO4=ZnSO4+H2↑
②金属与强碱溶液的置换反应:
单质+化合物化合物+单质:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
2.乙烯
(1)工业制法:
石油裂解制乙烯:高碳烷烃低碳烷烃+低碳烯烃:
C4H10=C2H6+C2H4 ;C8H18=C6H14+C2H4
(2)实验室制法:

乙醇的消去反应:CH3CH2OH = CH2=CH2 ↑+H2O
3.乙炔
(1)工业制法:
煤干馏得到焦炭,煅烧石灰石得到生石灰高温煅烧石灰石装置,在高温电弧炉中生石灰和焦炭反应生成电石和一氧化碳,电石和饱和食盐水反应生成熟石灰和乙炔。
3C+CaO = CaC2+CO↑ ;CaC2+2H2O=Ca(OH)2+C2H2 ↑
(2)实验室制法:电石水解法:CaC2+2H2O=Ca(OH)2+C2H2 ↑
4.一氧化碳
(1)工业制法:
①水煤气法:(高温条件下还原水蒸气)
单质+化合物化合物+单质: C+H2O(g)=CO+H2 ;
②焦炭还原二氧化硅(工业制备粗硅的副产物):2C+SiO2=Si+2CO↑
③工业制备电石的副产物:3C+CaO = CaC2+CO↑ ;
(2)实验室制法:
①草酸分解法:H2C2O4= CO↑ +CO2 ↑+H2O ;混合气体通过碱石灰得到一氧化碳。
②甲酸分解法:HCOOH = CO↑ +H2O
5.二氧化碳
(1)工业制法:

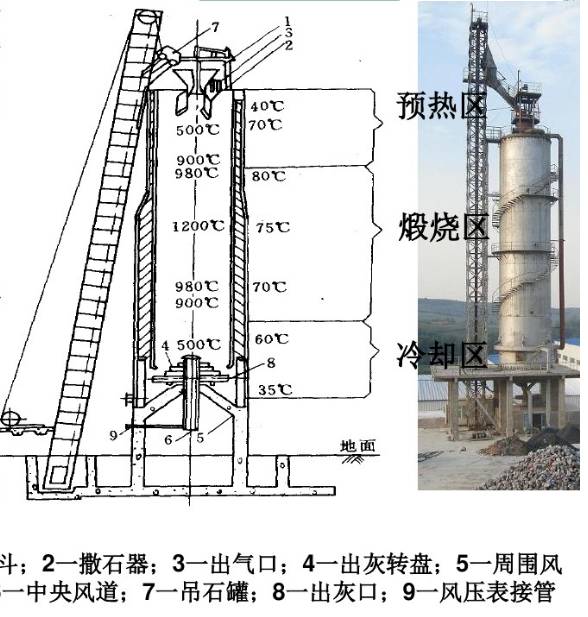
①高温分解,煅烧大理石:CaCO3=CaO+CO2 ↑
5-19利用本书附表与下列数据计算石灰岩[以 caco3 (方解石)计]被 co2 g 溶解发育成 喀斯特地形的如下反应的标准摩尔生成焓:caco3 s + co2 g + h2o l ca2+ aq +2hco3- aq △fhmθ/ kj.mol-1: ca2+ aq -543.0 hco3- aq -691.15-20火柴头中的p4s3 s 的标准摩尔燃烧热为-3677 kj.mol-1 [注:燃烧产物为 p4o10 s 和so2 ],利用本书附表的数据计算p4s3 s 的标准摩尔生成焓。《环境化学》 第三章 水环境化学大气中的co2 生物降解2008-5-12碳的循环光合作用溶解作用和化学过程固定的有机碳(ch2o) 和人为合成的碳溶解性的无机碳 主要为hco3-用石油原料生产 的异型生物质生物地球化 学过程以溶解的co2 的溶解作用化学沉淀作用 和无机碳结合 于微生物外壳固定的有机烃类高温煅烧石灰石装置,cxh2x 和油母页岩不溶性无机碳, 主要为caco3 和caco3·mgco321。石头的成分中含有caco3,空气中含有co2,它们会发生化学反应:caco3 +co2 +h2o==ca2生成溶于水的ca2。
③联碱工业小苏打制纯碱的副产物:2NaHCO3=Na2CO3+H2O+CO2 ↑
(2)实验室制法:
复分解反应:碳酸钙与盐酸的反应:CaCO3+2HCl=CaCl2+H2O+CO2↑
6.氨气
(1)工业制法
化合反应:合成氨工业N2+3H2=2NH3
(2)实验室制法
①氯化铵和消石灰混合受热分解制备氨气: 2NH4Cl+Ca(OH)2=CaCl2+2NH3 ↑+2H2O
②浓氨水滴入到生石灰(烧碱或碱石灰)表面快速产生氨气。
7.一氧化氮
(1)工业制法
①氨气催化氧化制备一氧化氮(硝酸工业的第一步反应):4NH3+5O2=4NO+6H2O
②二氧化氮溶于水制硝酸的副产物:3NO2+H2O=2HNO3+NO
(2)实验室制法
铜和稀硝酸反应制备一氧化氮:3Cu+8 HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O

8.二氧化氮
(1)工业制法
一氧化氮氧化制二氧化氮:(硝酸工业的第二步反应):2NO+O2=2NO2
(2)实验室制法
铜和浓硝酸反应制备二氧化氮:Cu+4 HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
9.氧气
(1)工业制法:
①分离液态空气
②电解氧化铝得到副产物氧气:2Al2O3=4Al+3O2 ↑
③冶炼金属汞、银时得到副产物氧气:2HgO=2Hg+O2↑;2Ag2O=4Ag+O2↑
(2)实验室制法
①高锰酸钾受热分解:2KMnO4=K2MnO4+MnO2+O2↑
②双氧水催化分解:2H2O2=2H2O+O2↑
10.二氧化硫
(1)工业制法
①高温煅烧硫铁矿得到二氧化硫:4FeS2+11O2=2Fe2O3+8SO2
②火法炼铜得到副产物二氧化硫:Cu2S+O2=2Cu+SO2

③燃烧硫磺得到二氧化硫:S+O2=SO2
(2)实验室制法
①在加热条件下铜还原浓硫酸:Cu+2H2SO4(浓) =CuSO4+SO2↑+2H2O
②亚硫酸钠和硫酸发生复分解反应:Na2SO3+ H2SO4=Na2SO4+H2O+SO2 ↑
11.氯气
(1)工业制法
①电解饱和食盐水得到烧碱、氢气和氯气:2NaCl+2H2O=2NaOH +H2↑+ Cl2↑
②冶炼钠时得到钠和氯气:2NaCl(熔融)=2Na + Cl2↑
③冶炼镁时得到镁和氯气:MgCl2=Mg + Cl2↑
(2)实验室制法
①常温氧化浓盐酸:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
②加热氧化浓盐酸:MnO2+4HCl(浓)= MnCl2+Cl2↑+2H2O
12.氯化氢
(1)工业制法
氢气在氯气中燃烧产生氯化氢:H2+Cl2=2HCl
(2)实验室制法
①复分解反应制备氯化氢气体:2NaCl+H2SO4(浓)= Na2SO4+2HCl ↑
②浓硫酸滴入到浓盐酸中快速制备氯化氢气体。
你傻不傻