实验室制备二氧化碳常用的方法是 [ ] A.煅烧石灰石 B.
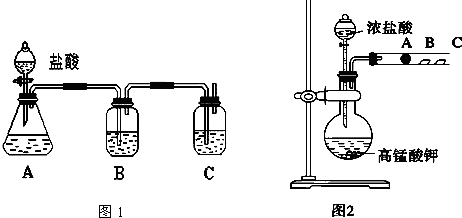
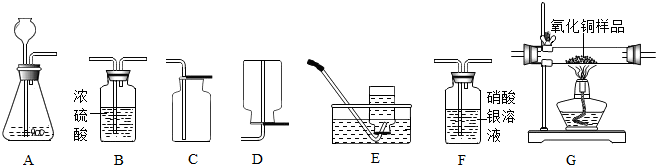
现有A、B、C、D、E五种装置,根据题意,将序号填人相应的空格中.
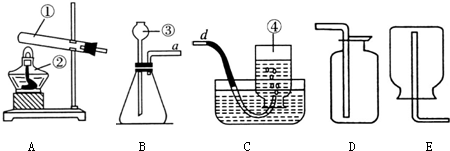
(1)实验室用加热高锰酸钾制备氧气用装置,收集氧气最好用装置.
(2)用石灰石与稀盐酸制备二氧化碳,用装置,收集用装置.
(3)氨气极易溶于水,且密度比空气小,实验室常采用加热固体硫酸铵和固体熟石灰的混合物来制备氨气,应选用的发生装置为,收集装置为,其反应的化学方程式为.
(一)必考题(共129分)22.(5分) 在利用碰撞做“验证动量守恒定律”的实验中,实验装置如图甲所示,图中斜槽部分与水平槽部分平滑连接,按要求安装好仪器后开始实验。解:(1)如图a甲所示 (2)如图a乙所示 【设计实验与进行实验】如图b所示 【评估】(1)换导线 换电池 (2)取下一个小灯泡,若另一个小灯泡还能发光,说明是并联,若不能发光,说明是串联。校化学兴的学根据验提供的仪器和药品,老师的指导下从如图中选择装置进了气的制备实验.。
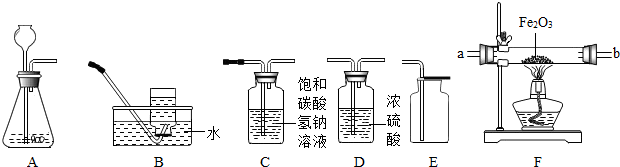
试根据题目要求,回答下列问题:(提示:3H2+Fe2O3
2Fe+3H2O)
(1)若在实验室中用稀盐酸与大理石制取并收集纯净、干燥的二氧化碳气体.(提示:盐酸中挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)
①所选仪器的连接顺序为(填仪器序号字母).
②制取气体的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.
③实验室制取二氧化碳后的剩余废液中,常含有剩余的少量盐酸,欲加入过量的药品除去盐酸,得到较纯净的中性液体,请从熟石灰、纯碱、石灰石三种固体药品中选用一种试剂进行实验,并简述操作方法
石灰石;加入过量的石灰石,充分反应后过滤,即得到较纯净的中性液体
石灰石;加入过量的石灰石,充分反应后过滤,即得到较纯净的中性液体
(2)欲用锌和稀硫酸反应制取氢气,并测定某不纯氧化铁样品中氧化铁的质量(杂质不反应),所选仪器的连接顺序为:A→D→F.
①实验时,会观察到装置F中的现象为
红色变黑色,试管壁上有水雾
红色变黑色,试管壁上有水雾
.
②若反应进行完全后,仪器F的质量减少ag,则氧化铁样品中的氧化铁的质量为g(计算结果可为分数形式).
③锌和稀硫酸反应后,所得溶液质量与之前相比会(填写下列各项序号)
A.增大;B.减小;C.不变;D.无法判断.
图1是实验室常用的装置,请回答下列问题:
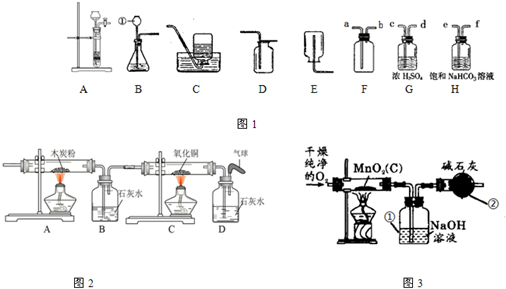
(1)写出仪器①的名称
长颈漏斗

长颈漏斗
.收集某气体能采用E装置,由此推测该气体具有的性质是
密度比空气小
密度比空气小
.
(2)实验室制备并收集氧气的装置组合是
A(或B)C(或D)
A(或B)C(或D)
(填装置序号),反应的化学方程式为
2H2O2
2H2O+O2↑
2H2O2
2H2O+O2↑
;若用F装置收集该气体,则气体应从端进入(填“a”或“b”);装置A、B都可以用来制取二氧化碳,比较这两个装置,指出A装置的一个突出优点是
可以随时控制反应的发生和停止
可以随时控制反应的发生和停止
.
(3)实验室制得的CO2气体中常含有HCl和水蒸气,为了得到纯净、干燥的CO2气体,除杂装置的导管气流方向连接顺序是(填选项字母编号).
A.c→d→e→fB.d→c→e→fC.e→f→c→dD.f→e→d→c
加热固体,若产生能使澄清石灰水变浑浊的气体,则原固体是nahco3,否则就是na2co3错误。如用澄清石灰水来鉴别氧气和二氧化碳时,不能直接说二氧化碳能使澄清的石灰水变浑浊,而应该说使澄清石灰水变浑浊(现象)的物质是二氧化碳(结论),无明显变化的物质是氧气。小白鼠呼吸吸收氧气呼出二氧化碳,氧气被小白鼠吸收掉,石灰水吸收了二氧化碳故容器内气体压强变小,u形管内液面会有变化a处上升b处下降故答案为:澄清石灰水变浑浊,上升,下降,木条熄灭高温煅烧石灰石装置,氧气,二氧化碳.。
一氧化碳和二氧化碳
一氧化碳和二氧化碳
,B处发生反应的化学方程式是
CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Ca(OH)2═CaCO3↓+H2O
.
⑵为测定固体a中二氧化锰的质量分数,兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使炭在加热条件下反应生成co2来进行分析测定(假设每步反应完全)。如何证明滤液c中含有氯化铵 ▲ ⑵为测定固体a中二氧化锰的质量分数,兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使炭在加热条件下反应生成co2来进行分析测定(假设每步反应完全)。如何证明滤液c中含有氯化铵 ▲⑵为测定固体a中二氧化锰的质量分数高温煅烧石灰石装置,兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使炭在加热条件下反应生成co2来进行分析测定(假设每步反应完全)。
①如图3所示是用干燥纯净的氧气与样品反应来测定二氧化锰质量分数的装置,仪器②中装有碱石灰(氧化钙和氢氧化钠的混合物),其作用是
吸收空气中的二氧化碳
吸收空气中的二氧化碳

.
②为验证装置①已将CO2吸收完全,可在装置①与②之间加入
盛有澄清石灰水的洗气瓶
盛有澄清石灰水的洗气瓶
装置进行证明.
根据质量守恒定律,由装置质量变化即为生成的二氧化碳的质量求得产生二氧化碳的质量,利用反应的化学方程式,由产生二氧化碳的质量求出样品中碳酸钠的质量而计算碳酸钠的质量分数.。(1)固体与液体反应后有关溶质质量分数的计算于固体与液体发生反应,求反应后溶液中溶质的质量分数,首先要明确生成溶液中的溶质是什么,其次再通过化学反应计算溶质质量是多少(有时溶质质量由几个部分组成),最后分析各量间的关系,求出溶液总质量,再运用公式计算出反应后溶液中溶质的质量分数。①装置a反应前后质量差m1②装置c反应前后质量差m2③装置d反应前后质量差m3 27.(14分)铁和铁的化合物在工业生产和日常生活中都有广泛的用途。
实验类型:综合实验要求:必修实验内容:(1)制备na[al oh 4],(2)氢氧化铝的生成和洗涤,(3)明矾的制备,(4)产品熔点的测定及性质实验。实验室制备二茂铁反应原理及装置示意图如下:Ⅰ.反应原理2koh+fecl2+2c5h6―→(c5h5)2fe+2kcl+2h2o(环戊二烯) (二茂铁)Ⅱ.实验装置Ⅲ.实验步骤步骤1.在三颈烧瓶中加入25 g粉末状的koh,并从仪器a中加入60 ml无水乙醚到烧瓶中,充分搅拌,同时通氮气约10 min(如图1)。全书共分十章,内容除绪言、实验室基本知识、实验数据处理、常用仪器及基本操作、实验基本操作等基本知识外,实验内容按照物理化学量及常数的测定,化学反应原理与物质结构基础,元素化合物的性质,无机化合物的提纯与制备、综合性、设计性和研究性实验等采用模块结构编写。
废盐酸石灰中和-上海破碎机厂家某同学称取石灰石样品,向其中加入足量的稀盐酸杂质不与稀盐酸反应待充分反映后,共收集到二氧化碳气体,试求该石灰石样品中碳酸钙的质量分数。常温下二氧化碳是一种无色有刺激性气味的气体,它的密度比空气大,二氧化碳能使高锰酸钾溶液褪色(二氧化碳不能).实验室常用亚硫酸钠(na2so3)固体与稀盐酸在常温下反应制取二氧化硫(na2so3+2hcl═2nacl+so2↑+h2o)(1)现用亚硫酸钠与稀盐酸制取二氧化硫,你选择的反应发生装置是(填“a”或“b”)。③小聪:碳酸钙和盐酸反应生成二氧化碳气体,氢氧化钙显碱性,能使酚酞变红.故答案为:取少量样品,加入足量水充分溶解,过滤.取少量滤渣于试管中,加入适量稀盐酸,冒气泡,说明含有caco3。
①所选仪器的连接顺序为(填写仪器序号字母).
②生成二氧化碳时,所发生反应的化学方程式为:
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.
③如果仪器F中出现
白色沉淀
白色沉淀
现象,则证明二氧化碳中混有氯化氢气体.
④实验室制取二氧化碳后的剩余废液中,常含有剩余的少量盐酸,欲验证盐酸的存在,请从AgNO3溶液、石蕊、Na2CO3溶液三种试剂中选用一种试剂进行验证,并简述选择的理由
选Na2CO3溶液,因为盐酸与碳酸钠反应有气泡冒出,现象明显
选Na2CO3溶液,因为盐酸与碳酸钠反应有气泡冒出,现象明显
.
(2)若仪器A中盛放Zn和H2SO4溶液,某同学欲利用制备的氢气来测定CuO样品中CuO的纯度(杂质不反应),仪器的连接顺序为A→G→B.(已知:CuO+H2
Cu+H2O)
①实验时,会观察到装置G中的黑色固体变成色.
②该同学通过测量反应前后B装置质量的增加,来计算样品中CuO的纯度,则计算结果会
偏大
偏大
(填“偏大”、“偏小”、“不受影响”之一).
请你根据提供的实验装置和药品,参与实验室气体制备的探究.


【提高药品】高锰酸钾、稀盐酸、大理石
【熟悉仪器】请填写标号仪器的名称:①
酒精灯
酒精灯
,②
分液漏斗
分液漏斗
.
【比较探究】根据所提供的药品,填写下表.
气体
反应物状态
反应条件
收集方法和依据
二氧化碳
固体和液体
常温
向上排空气法
CO2密度比空气大
氧气
固体
加热
排水法
不易溶于水
不易溶于水
向上排空气法
向上排空气法
O2密度比空气略大
【实践探究】
(1)用加热高锰酸钾的方法制取氧气,应选用的发生装置是(填字母编号),写出该反应的符号表达式

2KMnO4
K2MnO4+MnO2+O2↑
2KMnO4
K2MnO4+MnO2+O2↑
.
(2)下列是某同学用加热高锰酸钾制取氧气部分实验操作,其中不合理的是.
A.先检查装置的气密性,后加药品
B.先将导管伸入集气瓶,后加热试管
C.实验结束先将导管移出水面,后熄灭酒精灯
(3)实验室制取可用
BD或CD
BD或CD
装置组合(填字母编号)可制取二氧化碳,写出实验室制取二氧化碳的符号表达式
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.
【反思小结】气体制取和收集装置的选择依据:
收集装置的选择依据--气体的密度、气体在水中的溶解性,该气体能否与空气或水反应;发生装置的选择依据--
反应物状态
反应物状态
和
反应条件
反应条件
.
【拓展应用】实验室用锌粒和稀硫酸反应制取氢气,氢气常选用装置B或装置C,C与B相比较,其优点是
可控制反应的发生与停止
可控制反应的发生与停止
;
氢气是密度最小的气体,难溶于水,可选用的收集装置为
E或F
E或F
(填字母编号).
#易烊千玺献声小王子##易烊千玺#早安