原子的构成PPT课件

四 涉及氧传递的膜催化反应五 c1-化学中的膜催化转化第四节 展望参考文献第六章 催化剂的分子设计第一节 概述第二节 对分子设计的了解第三节 分子设计的基础一 理论化学和模拟二 分析仪器三 表面科学四 金属有机化学五 分子筛科学六 反应工程第四节 催化剂的设计――开创未来一 现有产品的可替代工艺的开发二 现有产品的新工艺的开发三。二氧化硅是硅原子跟四个氧原子形成的四面体结构的原子晶体,整个晶体又可以看作是一个巨大分子,sio2是最简式,并不表示单个分子。在压制过程中,虽然由于外力的作用能增加粉末体的接触面,而颗粒中表面原子和分子还是杂乱无章的,甚至还存在有内应力,颗粒间的联结力是很弱的,但烧结后颗粒表面接触状态发生了质的变化,这是由于粉末接触表面原子﹑分子进行化学反应,以及扩散、流动、晶粒长大等物理化学变化,使颗粒间接触紧密,内应力消除,制品形成了一个强的整体,从而使其性能大大提高。

1993年,中国科学院科学家通过移动单个硅原子所写成的世界上最小的“中国”两字。年,中国科学院科学家通过移动单个硅原子所写成的世界上最小的“中国”两字。这是中国科学家用一个个铁原子排列出的世界上最小的“原子”二字。这是中国科学家用一个个铁原子排列出的世界上最小的“原子”二字。这是中国科学家用一个个铁原子排列成的“原子”二字这是中国科学家用一个个铁原子排列成的“原子”二字扫描隧道显微镜下的金原子扫描隧道显微镜下的金原子扫描隧道显微镜下的金原子扫描隧道显微镜下的金原子扫描隧道显微镜下的金原子扫描隧道显微镜下的金原子有关原子的假设:公元前5世纪,希腊哲学家德谟克利特等人认为物质是由原子构成的,提出了原子的概念。世纪,希腊哲学家德谟克利特等人认为物质是由原子构成的,提出了原子的概念。19世纪初,英国科学家道尔顿提出近代原子学说,在科学界达成了共识。世纪初,英国科学家道尔顿提出近代原子学说,在科学界达成了共识。在哲学原子论、元素学说、质量守恒定律获得发展的的基础上,1803年英国科学家在哲学原子论、元素学说、质量守恒定律获得发展的的基础上,1803年英国科学家 道尔顿提出了近代科学原子论。

提出了近代科学原子论。道尔顿的近代原子学说1. 物质都由原子构成。2. 原子是微小的不可分割的实心球体。3. 同种元素的原子的性质和质量都相同。上述三个观点在今天看来都是不正确的。但这并不能抹杀道尔顿的贡献,他被称为近代化学的鼻祖但这并不能抹杀道尔顿的贡献,他被称为近代化学的鼻祖在化学变化中原子不可分, 道尔顿也认为原子是不可分割的实体,那么原子是否真的是不可再分的最小粒子呢?也认为原子是不可分割的实体,那么原子是否真的是不可再分的最小粒子呢?原子虽小,却还有原子核,那么,原子的结构到底怎样原子虽小,却还有原子核,那么,原子的结构到底怎样 ?我国成功爆炸第一颗原子弹的图片我国成功爆炸第一颗原子弹的图片1897年,英国科学家汤姆森发现了“电子”:年,英国科学家汤姆森发现了“电子”: 电子 带 负 电荷 , 是所有物质原子共有的组成部分。物质原子共有的组成部分。汤姆森1906年获诺贝尔物理学奖年获诺贝尔物理学奖电子的发现摧毁了“原子不可再分”的观念,打开了通往原子世界的大门,科学家们纷纷提出了自己的的发现摧毁了“原子不可再分”的观念,打开了通往原子世界的大门,科学家们纷纷提出了自己的 原子结构模型 ......汤姆森认为:原子是一个认为:原子是一个 平均 分布着 正电荷的粒子,其中的粒子原子的构成 ppt,其中 均匀 地镶嵌着许多 电子,中和了正电荷,从而形成了中性原子,人称,中和了正电荷,从而形成了中性原子,人称 枣糕式无核模型 (也有人称为西瓜西瓜 模型或 葡萄干布丁 模型)。
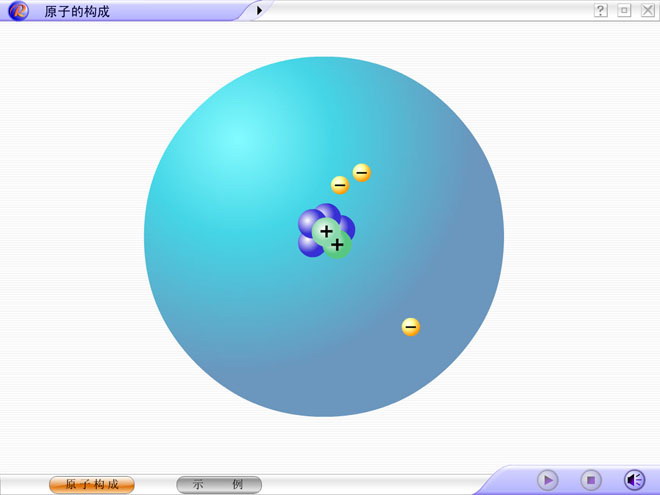
依据卢瑟福的原子行星模型理论,在原子中绕核高速旋转的是__。世界上的物质都是由原子构成的,原子则是由原子核和绕核高速运动的电子组成,原子核带正电,电子带负电。宇宙是由物质组成的,物质是由分子组成的原子的构成 ppt,分子是由原子组成的,原子是由位于中心的原子核和核外的电子组成的,原子核的质量比电子的大得多,几乎集中了原子的全部质量,原子核带正电,电子带负电,电子在原子核的吸引下,绕核高速运动。

有关原子的假设:卢瑟福提出了一个更完整的原子模型:有关原子的假设:卢瑟福提出了一个更完整的原子模型:1 、原子的中央是由很重的带正电的质子构成的核。2 、远离这个核的是很轻的带负电的电子。3 、电子绕着核转,像行星绕着太阳转一样。大宇宙和小宇宙的美是统一的行星绕太阳旋转1913年,丹麦科学家 玻尔提出了提出了 量子化的原子结构模型,即核外电子只能在限定的轨道内绕核运转,按能量高低而距离核远近不同,也因此,即核外电子只能在限定的轨道内绕核运转,按能量高低而距离核远近不同,也因此获得1922年的诺贝尔物理学奖。获得1922年的诺贝尔物理学奖。原子结构模型的演变原子原子核核外电子原子核核外电子质子中子质子中子1个质子带一个单位正电荷个质子带一个单位正电荷不带电一个电子带一个单位负电荷一个电子带一个单位负电荷( 0 )( + )( - )( + )( 0 )( 核电荷数)1个质子带一个单位正电荷1个电子带一个单位负电荷中子不带电个质子带一个单位正电荷1个电子带一个单位负电荷中子不带电若将 原子 比做一个庞大的 体育场 ,而原子核 只相当于一只 蚂蚁。原子的质量集中在原子核上,但是原子核的体积仅占原子体积的几千亿分之一.原子内部有一个很大的空间。
卢瑟福原子模型(又称行星原子模型):原子是由居于原子中心的带正电的原子核和核外带负电的电子构成。原子由居于原子中心带正电的原子核和周围带负电的电子构成,原子核由质子和中子两种微粒构成,但氢原子核只由一个质子构成。原子尽管很小,但具有一定的构成,是由居于原子中心的带正电的原子核和核外带负电的电子构成的。
2、答案 a 解析 分子或原子中质子数=核外电子数,阳离子中质子数=核外电子数+电荷数,阴离子中质子数=核外电子数-电荷数,同位素的不同核素具有相同的质子数和核外电子数。原子是由中心的带正电的原子核和核外带负电的电子构成的(反物质相反),原子核是由质子和中子两种粒子构成的,电子在核外较大空间内做高速运动。考点49 原子结构与性质(a卷)第i卷 选择题一、选择题1.35cl和 35cl- 两种微粒中,不同的是a.核内质子数b.核外电子层数c.核内中子数d.核外电子数【答案】d【解析】试题分析:a.35cl和 35cl-都是由氯元素形成的微粒,核内质子数均是17,a项不符,b.氯原子最外层有7个电子,得到一个电子形成8电子的稳定结构,核外电。