甘肃省武威市凉州区武威第八中学2019届高三上学期第三次统一考试化学试题
武威八中2019届高三年级第三次统一考试化学试题可能用到的相对原子质量:H-1 Cl -35.5 P - 31 Zn -65 Cu -64 Fe- 56O- 16 N- 14 Na -23 C- 12 Ba -137 S- 32第I卷 选择题部分,16小题每小题3分共48分一、选择题:(本题共16小题,每小题3分,共48分。每小题给出的四个选项中只有一个符合题目要求,按要求选出正确答案)1.中国传统文化对人类文明贡献巨大,古代文献中记载了古代化学研究成果。下列常见古诗文对应的化学知识正确的是( )选项古诗文化学知识A《本草纲目拾遗》中对强水的记载:“性最烈,能蚀五金,其水甚强,惟玻璃可盛高中化学喷泉实验。”强水为氢氟酸B《本草经集注》中记载鉴别硝石(KNO3)和朴硝(Na2SO4)的方法:“强烧之,紫青烟起,云是真硝石也。”利用焰色反应C《诗经·大雅·绵》:“堇茶如饴。”郑玄笺:“其所生菜,虽有性苦者,甘如饴也。”糖类均有甜味D《梦溪笔谈》中对宝剑的记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折。”铁 的 合 金 硬 度 比 纯 铁的大,熔点比纯铁的高2.化学与生活、环境密切相关,下列有关说法不正确的是()A.Na2O2 吸收 CO2 产生 O2,可用作呼吸面具供氧剂B.碘酸钾具有较强氧化性,在食盐中加入适量碘酸钾,可抗人体老化C.竹炭具有超强的吸附能力,可用于吸收新装修房屋内的有害气体D.研发使用高效电力能源汽车,减少雾霾污染以降低呼吸系统发病率3.某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。

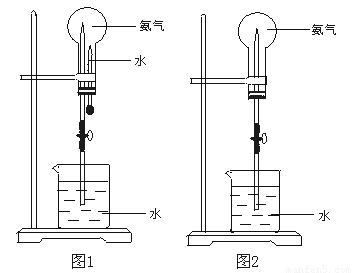
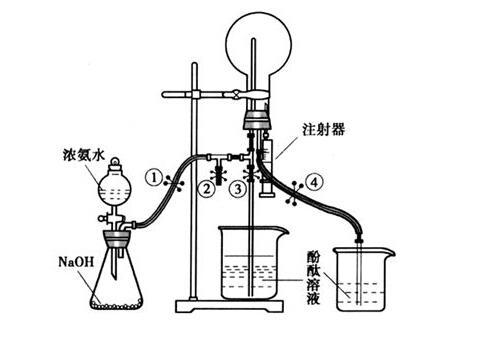
上述说法正确的是()A.①③④⑦B.①②⑤⑥C.③⑤⑥⑦D. ①②③④4.设 NA 为阿伏加德罗常数的数值高中化学喷泉实验。下列有关叙述一定正确的是()A.0.1 mol 苯完全转化为环己烷,破坏的碳碳双键总数为 0.3NAB.1 mol· L-1 的 CH3COONH4 溶液中含有的氧原子总数大于 2NAC.标准状况下,2.24 L 由 CO 和 N2 组成的混合气体中含有的原子总数为 0.2NAD. 4.6 g 钠用有小孔的铝箔包裹后与足量水充分反应生成 H2 的分子总数 为 0.1NA5.在同温同压下用排气法收集NH3和HCl进行喷泉实验(如图),下列说法错误的是(设Vm表示该条件下气体摩尔体积)()A. 所得溶液中溶质的物质的量浓度均为1/Vmmol·L−1B. “喷泉”结束时烧瓶内充满液体C. 图2可通过膨胀法引发“喷泉”D. 图1、图2中喷泉的颜色分别为蓝色、红色6.关于某无色透明溶液中所含离子的鉴别,下列叙述正确的是 ()A.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,则原溶液中一定有SO42—B.加入NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,C.加入盐酸,生成的气体能使饱和的澄清石灰水变浑浊,则原溶液中一定有CO32—D.通入Cl2后,溶液变为黄色,加入淀粉液后溶液变蓝,则原溶液中一定有I—则原溶液中一定有NH4+7.实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )A.装置①常用于分离互不相溶液体混合物B.以NH4HCO3为原料,装置③可用于实验室制备少量NH3C.装置②可用于吸收HCl气体,并防倒吸D.装置④b口进气可收集CO2、NO等气体8.、、和四种离子以物质的量之比2:4:1:1大量共存于同一溶液中,可能是()A.B.C. D.9.把含有和的混合溶液分成两等份,一份加入含a的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含 的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。

则原混合溶液中钾离子的浓度为( )A.B.C.D.10.25℃时,下列各组离子在指定溶液中一定能大量共存的是()A.0.1mol·L-1的NaAlO2溶液中:K+、H+、NO3-、SO42-B.0.1mol·L-1的Fe(NO3)2溶液中:Na+、H+、SCN-、I-C.由水电离产生的c(H+)=1×10-13mol·L-1的溶液中:Na+、Ba2+、NO3-、Cl-D.滴入石蕊试液显蓝色的溶液中:K+、Na+、HSO3-、ClO-11.下列化学反应的离子方程式正确的是()A.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO=CaSO4+H2OB.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3+2HClOC.用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2SD.在稀氨水中通入过量CO2: NH3·H2O+CO2=NH+HCO12.某溶液中可能含有H+、N、Mg2+、Al3+、Fe3+、C、S、N中的几种。①若加入锌粒,产生无色无味的气体。②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。

则下列说法正确的是( )A.溶液中的阳离子只有H+、Mg2+、Al3+B.溶液中一定不含C,可能含有S和N [来C.溶液中n(N)=0.2 molD.n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶113.A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大。已知:A和C、B和D分别位于同主族,且B、D质子数之和是A、C质子数之和的2倍。下列说法正确的是( )A. C的最高价氧化物对应水化物的碱性在同周期中最强B. 原子半径的大小顺序:r(B)>r(C)>r(D)C. E分别与A、C形成的化合物中化学键类型相同D. B的简单气态氢化物的热稳定性比D的弱14.向CuSO4 溶液中逐滴加入 KI 溶液至过量,观察到有沉淀(CuI)生成,且溶液变为棕色。再向反应后的混合物中不断通入SO2 气体,溶液逐渐变成无色。下列有关分析中正确的是()A.上述实验条件下,物质的氧化性Cu2+>SO2 >I2B. 在 SO2 与 I2 反应中得到的还原产物为 H2SO4C.通入SO2 后溶液逐渐变成无色,体现了 SO2 的漂白性D . 滴加 KI 溶液时,每转移 2mol e-会生成 2mol CuI 沉淀15、制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是( )A.烧杯中有铜无铁B.烧杯中有铁无铜C.烧杯中铁、铜都有D.烧杯中铁、铜都无16、在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末: ①; ②; ③; ④, 铜粉可溶解的是( )A.①②B. ①④C.②③D.②④第II卷 非选择题部分,共52分二、填空题17.(10分)下图分别代表有关反应中的一种物质,请填写以下空白。
【分析】本题是利用纤维素的水解产物葡萄糖氧化制备草酸的实验探究,结合反应速率的影响因素,水解时可适当提高温度,选择的硫酸溶液浓度不易太高,以防止因浓硫酸的脱水性使碎渣炭化,在葡萄糖的氧化过程中生成的氮氧物可以用氢氧化钠溶液吸收,产物可结合电子守恒和原子守恒进行计算,另外还考查了产物的分离提纯及干燥,最后利用滴定法分析了样品的纯度.。(1)求某一反应中被氧化与被还原的元素原子个数之比,或求氧化剂与还原剂的物质的量之比及氧化产物与还原产物的物质的量之比。感悟:从近3年全国i卷试题可以看出,生活中的化学、化学中的stse等基本上都是元素化合物知识的考查,广泛涉及具体物质的性质,3道选择题就涉及30多种物质的性质特点,考查到强氧化性酸与金属的反应、盐类水解与酯类水解、酸碱盐间的复分解反应、不稳定酸的分解反应、不活泼金属与盐溶液的氧化还原反应、侯氏制碱法的特殊反应、气体物质生成铵盐的化合反应、黑火药制备反应等10余种反应原理。
4