2018学年高一下学期3月月考化学试题

A.“PM2.5”与空气形成的分散系属于胶体
B.燃煤中加入生石灰不仅可以减少酸雨的形成及还可以减少温室气体的排放
C.汽车尾气中的氮氧化物是因为汽油不完全燃烧造成的
D.化学对社会发展与进步有巨大贡献,其中合成氨的主要贡献是解决了地球上粮食不足的问题
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:容易使用:148次加入试题篮收藏
【题文】下列说法正确的是
A.燃烧是指可燃物在氧气中发生的剧烈的发光发热的反应
B.黑火药由硫磺、硝石、木炭三种物质按一定比例混合制成
C.H2在O2中燃烧生成水与H2O电解生成H2和O2互为可逆反应
D.因为氨气与HCl气体可以形成NH4Cl固体,所以该反应属于氮的固定
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:容易使用:49次加入试题篮收藏
【题文】不法分子有时用铜锌合金制成假金币行骗。下列方法中,不能有效鉴别真假的是
A.在空气中灼烧看表面是否变黑
B.利用阿基米德原理测密度
C.用手掂量轻重
D.滴一滴硝酸在金币的表面,观察现象
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:容易使用:126次加入试题篮收藏
【题文】下列保存试剂的方法错误的是
A.漂白粉最好即买即用,购买后应该密闭保存在干燥的地方
B.氢氟酸(HF)保存在无色的玻璃瓶中
C.氢氧化钠溶液保存在带橡皮塞的玻璃瓶中
D.浓硝酸保存在棕色玻璃瓶中
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:较易使用:102次加入试题篮收藏
【题文】下列实验操作正确的是
A.教材上铜和浓硫酸实验,最后操作是先向上拉铜丝,终止反应,冷却后,把试管里面的液体慢慢倒入盛有少量水的另一支试管里,观察溶液颜色中颜色的变化
B.用润湿的淀粉碘化钾试纸鉴别Br2(g)和NO2
C.用加热法去除NaHCO3固体中得NH4Cl 固体
D.用玻璃棒蘸取新制氯水点在pH试纸正中测新制氯水的pH
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:较易使用:94次加入试题篮收藏
【题文】设NA为阿伏加德罗常数的值。下列说法正确的是

[0026]所述的催化空气氧化是指,先加热草甘膦母液到120°c,进入反应器,反应器内设置有催化触媒及加热电炉,反应温度为250°c,反应压力为6mpa,液空比为1:150,反应时间为 lomin。[0023]所述的催化空气氧化是指,先加热草甘膦母液到115°c,进入反应器,反应器内设置有催化触媒及加热电炉,反应温度为300°c,反应压力为9mpa,液空比为1:200,反应时间为 5min。[0021]所述的催化空气氧化是指,先加热草甘膦母液到110°c,进入反应器,反应器内设置有催化触媒及加热电炉,反应温度为200v,反应压力为5mpa,液空比为1:120,反应时间为 15min。
(5)银和稀、浓硝酸反应,方程式分别为:3ag+4hno3(稀)=3agno3+no↑+2h2o,ag+2hno3(浓)=agno3+no2↑+2h2o,对比两方法:若同样生成3molagno3,用银和稀硝酸反应,消耗4molhno3,生成1molno,用银和浓硝酸反应,消耗6molhno3,生成3molno2,即生成等物质的量的agno3时,消耗稀硝酸比浓硝酸少,同时产生的污染气体少。Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol。b.已知caco3与稀硝酸反应生成co2,推测caso3与稀硝酸反应生成so2。
C.标准状况下,22.4 L CS2中含有CS2分子数为NA
D.常温常压下,28g的N2和CO混合气体含有的原子数为2NA
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:较易使用:159次加入试题篮收藏
【题文】若箭头表示能直接一步转化,下列选项所示的物质间转化均能实现的是
A.Cl2 NaClO
NaClO NaCl
NaCl NaHCO3
NaHCO3
B.S SO3
SO3 H2SO4
H2SO4 CuSO4
CuSO4
C.N2 NO2
NO2 HNO3
HNO3 Fe(NO3)2
Fe(NO3)2
D.Si SiO2
SiO2 H2SiO3
H2SiO3 Na2SiO3
Na2SiO3
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:较易使用:131次加入试题篮收藏
【题文】如图为常见玻璃仪器组成的六种实验装置,根据需要加入液体或者固体试剂。高中化学喷泉实验下列说法错误的是( )
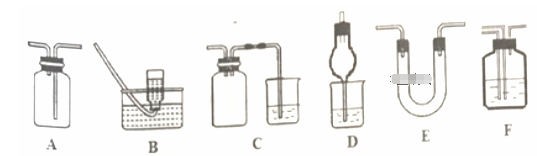
A. 装有P2O5固体的E不能用于干燥氨气
B. A、B装置能用于收集Cl2,又能用于收集NO
C. C、D装置可以用于尾气处理,能防止液体倒吸到气体发生装置中
5.2液体流程浓氨水由浓氨水泵从吸氨岗位浓氨水槽打入付塔,一方面溶解塔内的结疤,另一方面吸收主塔尾气中的剩余二氧化碳,逐步提高浓氨水的碳化度。 (da-100m密度计) (在工业测定中可以忽略为水的密度) 硫酸滴定法——化工部标准hg1-88-81《氨水》 5、结果计算 其中: c1—硫酸标准滴定溶液浓度,mol/l v1—硫酸标准滴定溶液消耗体积,ml v—取样体积,ml d —样品密度,g/ml 17.03 —氨的摩尔质量,g/mol 硫酸滴定法——化工部标准hg1-88-81《氨水》 注意事项:(1)取样后应立即分析,以免样品挥发使结果偏低。(9)无机酸制造业:三氧化硫吸收、塔式硫酸合成、间接浓硝、氯化氢干燥、过氧乙酸合成、硼酸合成、氢氟酸合成、磷酸合成。
难度:较易使用:62次加入试题篮收藏
【题文】下列离子方程式书写错误的是
A.NH4HCO3溶液中滴入少量稀NaOH溶液:NH4++HCO3-+2OH-=NH3·H2O+CO32-+ H2O
B.将Cl2通入到Na2SO3溶液中:Cl2+SO32-+H2O=SO42-+2H++2Cl-
C.向Na2SiO3溶液中通入过量CO2气体: SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-
D.Cu和浓HNO3的反应: Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:一般使用:110次加入试题篮收藏
【题文】将32g铜与150 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。则下列说法不正确的是
A.NO的体积为5.6L
B.该反应过程中共转移的电子数为NA
C.原硝酸溶液的浓度一定为10 mol/L
D.若用O2将生成的11.2LNO、NO2混合气体完全氧化HNO3,则所需O2的物质的量为0.25mol
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:较难使用:204次加入试题篮收藏
【题文】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

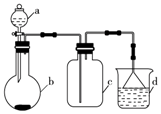
a中的物质
b中的物质
c中的物质
d中的物质
浓氨水
碱石灰
浓硫酸
CuSO4溶液
稀盐酸
NaOH溶液
浓盐酸
NaOH溶液
A.A
B.B
C.C
D.D
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:一般使用:164次加入试题篮收藏
【题文】某化学学习小组在帮助老师整理实验室的化学试剂时,发现一瓶无色溶液,标签破损如下图,据老师回忆,该药品应该是中学化学常用试剂。该小组同学根据已掌握的知识,对溶液进行鉴定。下列说法错误的是
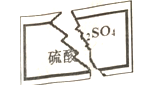
A.该小组同学推测它的阳离子可能是H+、Na+、K+、NH4+中的某一个
B.若要证明阳离子是否为NH4+,其方法是: 取少量溶液于试管中加稀NaOH溶液,若产生能使湿润的红色石蕊试纸变蓝的气体,则阳离子为NH4+
C.某同学操作时不慎将一滴溶液滴落在纸上,纸变黑,说明该溶液为浓硫酸
D.验证阳离子是否为Na+或者K+的实验方法是焰色反应
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:较易使用:67次加入试题篮收藏
【题文】喷泉是一种常见的现象,其产生原因是存在压强差。下面是某同学设计的四个不同的喷泉装置,则以下说法不正确的是

A.若向图1烧瓶中充满HI(与HCl水溶性相似)气体,烧杯中加入AgNO3溶液,则可以产生黄色喷泉
B.若向图2锥形瓶中加水,烧瓶中充满SO2,引发喷泉的操作是捂热上方的圆底烧瓶
C.若向图3装置的水槽中加入冰块或慢慢滴入浓硫酸都可以形成喷泉
但是在这个装置中,关闭装置24和34都是可以主动地控制,目的是将各关闭装置24和34保持在关闭或者打开状态,而不用管在各关闭装置处的流的状态。将体积不超过30 oml 的滤液加热至 50“c,倒入漏斗 (e) 中,把活塞 (c) 接到二氧 化 碳 源 或氮气源,通3 m in 惰性气体,并关闭活塞 (b) 及 (c).在拆除惰性气体源后,把固定在架上 的整个仪器取下,在活塞都关闭下,握住仪器剧烈摇动 5 m in,生成三价钦的 特性紫色后,垂直握住化工标准化与质量监督 1994年第 5期仪器,打开 活塞 (d) 并让锌汞齐流 至烧瓶(g ) 中.进行此操作要小心。操作:检查装置的气密性.装药品,连好仪器.夹紧弹簧夹,加热白磷,观察试管中所发生现象为_________.燃烧结束,试管冷却后打开弹簧夹,可以看到活塞慢慢左移到约_________刻度处(取整数值).说明空气中氧气的体积分数约为_________.。
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:较易使用:101次加入试题篮收藏

(2)葡萄糖遇浓hno3会氧化生成草酸,同时得到还原产物为no2和no且n(no2):n(no)=3:1,可根据电子守恒写出此反应的化学方程式,生成的混合气体被naoh溶液完全吸收,同样可根据原子守恒和电子守恒计算出两种盐n(nano2):n(nano3)。(2)该反应中,1molkio 3 的碘元素被还原生成0.5mol还原产物碘单质,同时会氧化5mol碘化钾生成0.25mol氧化产物碘单质,反应中做氧化剂.5=0,生成3mol碘单质会转移5mol电子,所以生成0.3mol碘单质需要转移0.5n a ,。(2)在催化剂的作用下,利用硝酸溶液氧化葡萄糖得草酸,同时还原产物为为no2和no且n(no2):n(no)=3:1,结合电离守恒、原子守恒及电荷守恒可得此反应的离子方程式为c6h12o6+12h++12no3﹣3h2c2o4+9h2o+3no↑+9no2↑,将反应后的混合气体用氢氧化钠溶液吸收,生成了nano2和nano3,发生反应的化学方程式为。
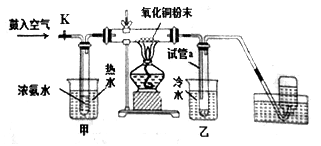
假定,测定铜的相对原子质量的实验过程中,氧化铜充分反应。以下叙述错误的是
A.关闭K的情况下完成实验,测得试管最终收集到的液体质量和氧化铜的质量可以求出铜的相对原子质量
臭氧的基本知识及其应用目 录臭氧的基本知识(一)臭氧与氧气对比(二)臭氧的氧化性能(三)臭氧的比较(四)臭氧的浓度臭氧的产生方法(一)基本方法(二)电晕放电臭氧发生器apl系列臭氧发生器臭氧的应用(一)自来水厂水处理(二)居民小区二次供水(三)臭氧在矿泉水、纯净水及饮料用水中应(四)游泳池水消毒灭菌(五)中水回用(六)制药厂如何选择用臭氧发生器(七)冷库消毒臭氧的基本知识(一)臭氧与氧气对比名称 臭氧 氧气 化学式 o3 o2 分子量 48 32 颜色 淡蓝色 无色 气味 特殊臭味 无味 常温状态 气体 气体 熔点 -251℃ -218.4℃ 沸点 -112.4℃ -183℃ 化学性质 臭氧比氧气更活泼 水中溶解度 臭氧的溶解度是氧的13倍 用途 消毒、灭菌、脱色、去臭 供给呼吸、支持燃烧 (二)臭氧的氧化性能下表为几种常用的氧化剂的氧化性能比较氧化剂 氧化性能eop eop/氯气eop 氟 3.06 2.25 臭氧 2.08 1.52 氯气 1.36 1.00 二氧化氯 1.27 0.93 (三)臭氧的比较臭氧是氧的同素导形体,即由同一类原子构成。稀有气体元素之一,无色,无臭,无味,气体密度0.9092克/升,液体密度1.204克/立方厘米,熔点-248.67℃,沸点-245.9℃,化学性质极不活泼,电离能21.564电子伏特,不能燃烧,也不助燃,在一般情况下不生成化合物,气态氖为单原子分子,氖还有一个特殊性质是气体与液体体积之比,大多数深冷液态气体在室温条件下产生500到800体积的气体,而氖则生成大于1400体积的气体。测量气体时流体温度变化,不像体积流量仪表那样气体体积变化改变所测(体积)流量,并不影响质量流量,然而如前文所述若温度变化过大,比热容的变化会导致量程变化。