下列物质中.哪些形成分子内氢键.哪些形成分子间氢键?

p σ键d.ch4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个c—h σ键解析:选dbf3为平面三角形,nh为正四面体,ch4分子中碳原子的2s轨道与2p轨道形成4个sp3杂化轨道,然后与氢原子的1s轨道重叠,形成4个sp3。由反应知道生成物应该是hcl,它是由一个氢和一个氯原子构成,且每一个氢分子、一个氯分子要生成两个hcl分子。h3bo3晶体是分子晶体,相互之间通过氢键相连,每个b原子形成三个b-o极性键,每个o原子形成o-h共价键,共6个键。
(1)下列物质中,哪些形成分子内氢键,哪些形成分子间氢键?(填序号)
①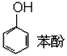 ②
② ③
③ ④
④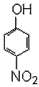 ⑤
⑤ ⑥
⑥
⑦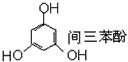 ⑧
⑧ ⑨HNO3 ⑩NH3
⑨HNO3 ⑩NH3
形成分子内氢键的有________;形成分子间氢键有________
(2)二聚甲酸解聚反应为:(HCOOH)2 → 2HCOOH,该反应需吸收60KJ/mol的能量,此能量是断开
_________键所需的能量,所以此键的键能为___________KJ/mol。
1、氢键的定义:是由已经与电负性很强的原子形成共价键的氢原子(如水分子中的氢)与另一个分子中电负性很强的原子(n、o、f)之间的作用力。下列说法错误的是a. 元素w、x的氯化物中,各原子均满足8电子的稳定结构b. 元素x与氢形成的原子比为1:1的化合物有很多种c. 元素y的单质与氢氧化钠溶液或盐酸反应均有氢气生成d.元素z可与元素x形成共价化合物xz2【解析】 本题考查物质结构、元素周期律的知识,意在考查考生对物质结构的推断能力、元素周期律的应用能力。分析:如果化合物中元素的最外层电子数+化合价的绝对值=8,则该元素满足8电子稳定结构,否则不是.解答:解:a、水分子中,氢原子最外层有2个电子,所以氢原子不满足8电子稳定结构,故a错误.b、氨气分子中,氢原子最外层有2个电子,所以氢原子不满足8电子稳定结构,故b错误.c、氯气分子中,氯原子最外层有7个电子,两个原子共用1个电子对使两个原子都达到8电子稳定结构,故c正确.d、氯化硼中,硼原子最外层有6个电子,所以硼原子最外层不满足8电子稳定结构,故d错误.故选c.点评:本题考查了8电子稳定结构的判断,难度不大,注意根据“化合物中元素的最外层电子数+化合价的绝对值=8,则该元素满足8电子稳定结构,否则不是”判断即可.。
查看习题详情和答案>>

(1)下列物质中,哪些形成分子内氢键,哪些形成分子间氢键?(填序号)

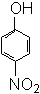
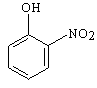

⑨HNO3 ⑩NH3
形成分子内氢键的有 ;形成分子间氢键有
27.【答案】(1)5(2)0.034(3)ac(4)h2s+co32-=hs-+hco3- c(na+)>c(hs-)>c(oh-) >c(h+)>c(s2-)(5)10-35 2.5×10-13【解析】(1) Δh=反应物断键吸收的总能量-生成物成键放出的总能量=1321+440-680-1076=5 kj·mol-1。③发生反应时,断开反应物的化学键吸收的总能量大于生成生成物时形成新化学键放出的总能量。d.反应热就是断键吸收的热量与成键释放的能量的差值,由于该反应吸热,所以反应中断开化学键吸收的总能量高于形成化学键放出的总能量。
分析:如果化合物中元素的最外层电子数+化合价的绝对值=8,则该元素满足8电子稳定结构,否则不是.解答:解:a、水分子中,氢原子最外层有2个电子,所以氢原子不满足8电子稳定结构,故a错误.b、氨气分子中,氢原子最外层有2个电子,所以氢原子不满足8电子稳定结构,故b错误.c、氯气分子中,氯原子最外层有7个电子,两个原子共用1个电子对使两个原子都达到8电子稳定结构,故c正确.d、氯化硼中,硼原子最外层有6个电子,所以硼原子最外层不满足8电子稳定结构,故d错误.故选c.点评:本题考查了8电子稳定结构的判断,难度不大,注意根据“化合物中元素的最外层电子数+化合价的绝对值=8,则该元素满足8电子稳定结构,否则不是”判断即可.。看图可知丙氨酸分子的化学式应该是c3h7o2n,一个丙氨酸分子中质子数是各个原子中子数之和,应该是44,丙氨酸中氮元素与氢元素的质量比为14:7就是2:1。p σ键d.ch4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个c—h σ键解析:选dbf3为平面三角形,nh为正四面体,ch4分子中碳原子的2s轨道与2p轨道形成4个sp3杂化轨道,然后与氢原子的1s轨道重叠,形成4个sp3。
查看习题详情和答案>>
但如果战争爆发我会第一时间到战地医院去