胶体的一些概念解释
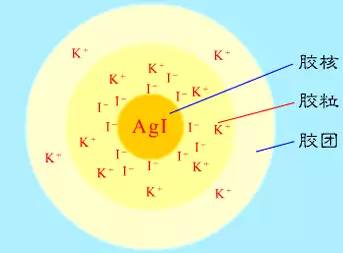
胶体的一些概念解释 1 胶团的结构 先有一定量的难溶物分子聚结形成胶粒的中心, 称为胶核。 胶核是固相, 有很大的表面积, 具有选择吸附离子的能力。 胶核选择吸附某一种离子, 形成紧密吸附层; 由于正、 负电荷相吸, 在紧密层外形成反号离子的包围圈, 从而形成了带与紧密层相同电荷的胶粒。 胶粒与扩散层中的反号离子, 形成一个电中性的胶团。 胶核吸附离子是有选择性的, 首先吸附与胶核中相同的某种离子或能与胶核表面反应生成难溶化合物的离子。 若无相同离子, 则首先吸附水化能力较弱的负离子。 除了 选择吸附导致胶粒表面带电之外, 有些溶胶胶粒表面带电则是离解的原因。 如: SiO2溶胶在不同 pH 溶液中水解时, 其胶粒可能带负电荷或正电荷。2.溶胶的聚沉 聚沉 在胶体中加入少量电解质后电解质电离产生的离子中和了胶体粒子所带的电荷, 使胶体粒子聚集长大, 形成的颗粒较大的沉淀会从分散剂里析出, 这个过程叫做聚沉。 原理 聚沉(Coagulation)。 胶体稳定的原因是胶粒带有某种相同的电荷互相排斥, 胶粒间无规则的布朗运动也使胶粒稳定。 因此, 要使胶体聚沉、 其原理就是:中和胶粒的电荷或加快其胶粒的热运动以增加胶粒的结合机会 常见方法 ①加快其胶粒的热运动以增加胶粒的结合机会, 使胶粒聚集而沉淀下来。
主要方式为加热胶体。②加入电解质。豆浆胶体带什么电荷 在胶体中加入电解质, 这就增加了胶体中与胶粒电性相反的粒子的浓度, 而给带电荷的胶体粒子创造了吸引相反电荷离子的有利条件, 从而减少或中和原来胶粒所带电荷, 使它们失去了保持稳定的因素。 这时由于粒子的布朗运动, 在相互碰撞时, 就可以聚集起来。 迅速沉降。 电荷 和相反电荷胶粒的胶体混合可以使胶体聚沉 加入盐 向胶体中加入盐时, 其中的阳离子或阴离子能中和分散质微粒所带的电荷, 从而使分散质聚集成较大的微粒, 在重力作用下形成沉淀析出。 这种胶体形成沉淀析出的现象称为胶体的聚沉(适用于液溶胶)。 形成胶冻状的豆腐 如由豆浆做豆腐时, 在一定温度下, 加入 CaSO4(或其他电解质溶液), 豆浆中的胶体粒子带的电荷被中和, 其中的粒子很快聚集而形成胶冻状的豆腐(称为凝胶)。一般说来, 在加入电解质时, 高价离子比低价离子使胶体凝聚的效率大。 如: 聚沉能力: Fe(3+)>Ca(2+)>Na(+), PO4(3-)>SO4(2-)>Cl(1-)。 胶体聚沉 影响溶胶稳定性的因素是多方面的, 例如电解质的作用, 胶体的相互作用等。

(1) 外加电解质对溶胶聚沉的影响溶胶受电解质的影响非常敏感, 通常用聚沉值来表示电解质的聚沉能力。 聚沉值是使一定量的溶胶在一定时间内完全聚沉所需电解质的最小的物质的量浓度。 ①舒尔策-哈迪价数规则: 聚沉能力主要决定于与胶粒带相反电荷的电解质离子价数,不同 价数( 1 、 2、 3 价) 的 反离子, 其聚沉值的 比 例 大约 为 100: 1.6:0.14, 约 为(1/1)^6:(1/2)^6:(1/3)^6, 即聚沉值与反离子价数的六次方成反比。 ②价数相同的离子聚沉能力 也 有所不同 。 例 如 , 一些一价正离子对负 溶胶的 聚沉能力 可以 排成如 下次序:H+>Cs+>Rb+>NH4+>K+>Na+>Li+而不同的一价负离子对正溶胶的聚沉能力则有如下次序: F->Cl->Br->NO3->I->SCN->OH-③同号离子对聚沉也有影响, 这是因为同号离子与胶粒之间的强烈的范德华力而产生吸附, 从而改变了胶粒的表面性能, 降低了反离子的聚沉能力。(2) 胶体的相互作用将胶粒带相反电荷的溶胶互相混合, 也会发生聚沉。

造纸废水净水剂是无机混凝剂,具有极强的催氧化及高效混凝功效,其在水解过程中产生大量的多核配合物,在进行废水处理时一方面起到防腐作用,另一方面通过静电中和及胶体吸附等共同作用,使废水中的胶体粒子脱稳,产生致密的凝聚实体,改善污泥回用在网部的留着和滤水性能。金属水合氧化物 (如氧化铝)在溶液中电解产生金属离子. 在适宜的 ph 值时发生矿物表面羟基化形成一系列金属氢氧化物以及多羟基金属水合氧化物,表面羟基功能基的存在使之强大的亲和力,通过共价键化学吸附、静电吸附和离子交换吸'附等作用发挥羟基的交换作用,吸附、固定氟化物。若有曝气,还会发生下面的反应:o2+ 4h+ + 4e→ 2h2o e(o2)=1.23vo2+ 2h2o + 4e → 4oh-e(o2/oh-)=0.41vfe2+ + o2 + 4h+ → 2h2o + fe3+反应中生成的oh-是出水ph值升高的原因,而由fe2+氧化生成的fe3+逐渐水解生成聚合度大的fe(oh)3胶体絮凝剂,可以有效地吸附、凝聚水中的悬浮物及重金属离子,且吸附性能远远高于一般的fe(oh)3,从而增强对废水的净化效果。
“美国伟大的国家”