(1)用图中甲装置进行喷泉实验.上部烧瓶已装满氨气.引起水上

乙酸和乙醇在硫酸存在下加热酯化后。乙酸钠或乙酸钾和乙醇在硫酸存在下蒸馏而得。醚化后的酚类混合物溶于50%乙醇中,再加入少量硫酸回流加热使其水解生成浓馥香兰素及类异丁香酚。
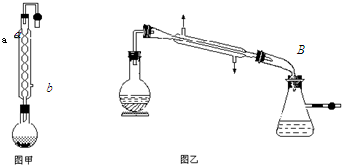
请回答下列问题:
(1)图甲中冷凝水从(a或b)进,图乙中B装置的名称为.
(2)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入,目的是.
(3)反应中加入过量的乙醇,目的是.
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:
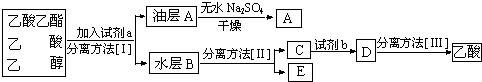
则试剂a是:,分离方法I是,分离方法II是,
试剂b是,分离方法III是.
(5)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯得到乙酸乙酯,在未用指示剂的情况下,他们都是先加NaOH溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来.甲、乙两人蒸馏产物结果如下:甲得到了显酸性的酯的混合物,乙得到了大量水溶性的物质.丙同学分析了上述实验目标产物后认为上述实验没有成功.
试解答下列问题:
①甲实验失败的原因是:
②乙实验失败的原因是:.

 如图所示装置,在化学实验中十分常见,它可以作为制取气体、收集气体、性质验证、安全防护等多种作用,按要求回答相关问题:
如图所示装置,在化学实验中十分常见,它可以作为制取气体、收集气体、性质验证、安全防护等多种作用,按要求回答相关问题:
(1)干燥CO2气体时,广口瓶中可装入的试剂1是
浓硫酸
浓硫酸
.
(2)除掉CO中混有的CO2,可以在广口瓶中盛装试剂2溶液.
(3)用此装置可以用排气法收集CO2气体,应从导管口进出.(填a或b)
如果用此装置收集CO气体,应怎样操作,简述操作方法:
将广口瓶盛满水,从a端通入气体,水从b端排出
将广口瓶盛满水,从a端通入气体,水从b端排出
.
(4)广口瓶C中盛有BaCl2溶液,如果从b端通入CO2气体,甲同学说有沉淀生成,乙同学说没有沉淀出现.根据你所掌握的知识高中化学喷泉实验,判断其正确性,选择你同意的一方意见回答相关问题(两项全答计0分).
I.我同意甲同学意见,得到的沉淀物质化学式为
无沉淀

无沉淀
.
II.我同意乙同学意见,如要出现沉淀,可以预先在广口瓶中加入一些试剂3,再通入CO2气体,立即会出现沉淀,则试剂3可以是
NaOH溶液
NaOH溶液
(填试剂名称或化学式).
某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如图1所示的实验装置.
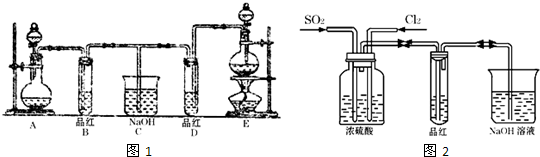
(1)实验室常选用制CO2的发生装置制SO2,实验室用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中装置(填装置序号)制Cl2,通过
分液漏斗
分液漏斗
(填写仪器名称)向烧瓶中加入适量的浓盐酸,反应离子方程式为.
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:
溶液由无色变成红色

溶液由无色变成红色
,D:
溶液没有明显变化
溶液没有明显变化
.
(3)甲乙两名同学分别利用如图2所示装置探究两种气体按不同比例混合后的漂白性.试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:
使两种气体充分混合,通过观察气泡的速度控制气体流量,使二者按一定比列混合
使两种气体充分混合,通过观察气泡的速度控制气体流量,使二者按一定比列混合
.
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:
(3)由图像可以看出,45g固体粉爪与100ml稀硫酸恰好完全反应生成co211l, 11lco2的质量为l1l×2g/l=22g,根据co2的质量可计算出100ml稀硫酸中硫酸的质量:由100ml 稀硫酸能与45g固体粉末完全反应,可计算出120ml 稀硫酸能与54g固体粉未完全反应,而加入的固体粉末为58.5g,则固体粉末有剩余,稀硫酸完全反应生成co2气体11l,则120ml稀硫酸与54g固体粉末完全反应生成二氧化碳的体积为:。基于这一发现,人们研究了能促使双氧水有效分解的活化剂,至今被研究过的双氧水漂白活化剂不外数十种,按活化剂的反应机理,活化剂大致可分为两大类,第一类是酰基化合物,其代表产品是乙二胺与醋酐反应的产物四乙酰乙二胺(taed)和壬基酰氧基苯磺酸钠(nobs),它们在与双氧水反应后生成相应的过氧羧酸,若生成的过氧羧酸是亲水性的,则称之为亲水性活化剂,如taed生成的是过氧乙酸,为水溶性。3.氧化物在反应物中、生成物中均写成化学式或分子式.4.浓h2so4作为反应物和固体反应时,浓h2so4写成化学式.5金属、非金属单质,无论在反应物、生成物中均写成化学式.微溶物作为反应物时,处于澄清溶液中时写成离子形式。
SO2和Cl2按1:1进气,二者恰好完全反应,生成无漂白性的H2SO4和HCl,SO2+Cl2+2H2O═H2SO4+2HCl
(结合反应方程式).

(2013?湖州二模)图甲是一种光化学电池高中化学喷泉实验,当光照在表面涂有氯化银的银片上时,AgCl(s)
Ag(s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-→Cl-(aq).图乙为可充电电池,溶液中c(H+)=2.0mol?L-1,阴离子为SO42-,a、b均为惰性电极,充电时右槽溶液颜色由绿色变为紫色.下列相关说法中不正确的是()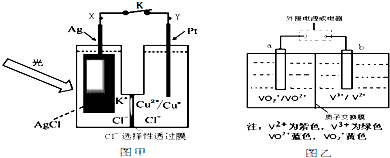
实验室制取苯甲酸甲酯用苯甲酸和甲醇为原料,已知苯甲酸、甲醇、苯甲酸甲酯、浓硫酸的有关性质如下表所示:
密度/g·cm-3
沸点/℃
溶解性
苯甲酸
微溶于水、易溶于有机溶剂
易溶于水、易溶于有机溶剂
苯甲酸甲酯
难溶于水、易溶于有机溶剂
易溶于水
(1)某同学用如下图一所示的装置制备苯甲酸甲酯,结果发现锥形瓶中没有收集到苯甲酸甲酯,原因是____________________________________________________________________。
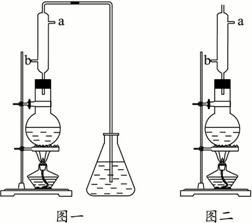
(2)该同学在分析实验失败的原因后,决定改用图二的装置进行,向烧瓶中加入浓硫酸、15 g苯甲酸、20 mL甲醇和_________________,冷却水从_________________处进。
主要用途:盛取液体或固体试剂.加热少量固体或液体. 制取少量气体反应器. 收集少量气体用. 溶解少量气体。同时上部不断注入铝液,这样在固体铝与液体铝之间有一个半凝固区.由于铝液在冷凝时要收缩,加上结晶器内壁有一层润滑油,随着底盘的下降,凝固的铝退出结晶器,在结晶器下部还有一圈冷却水眼,冷却水可以喷到已脱出的铝锭表面,为二次冷却,一直到整根线锭铸完为止。离心过滤是使悬浮液在离心力场下产生的离心压力,作用在过滤介质上,使液体通过过滤介质成为滤液,而固体颗粒被截留在过滤介质表面,从而实现液-固分离。
(4)将滤液倒入蒸馏装置中进行蒸馏,温度计应如何放置______________________________。
例如 韩束面膜背后的成分列表如下:苯氧乙醇 和 甲基异噻唑啉酮 就是令人恐慌的防腐剂了,常见防腐剂 名称以及危害:苯甲酸甲脂 methylparaben(也叫对羟基苯甲酸甲酯, 羟苯甲酯, 尼泊金甲酯, 对烃基苯甲酸甲酯) 与这个防腐剂类似的还有羟苯乙酯、羟苯丙酯、羟苯丁酯、尼泊金异丁酯等防腐剂。2-甲基呋喃、2-甲基庚烷、甲基环己烷、甲基环戊烷、甲基磺酸、2-甲基喹啉、4-甲基喹啉、8-甲基喹啉、n-甲基吗啉、1-甲基萘、2-甲基萘、2-甲基哌啶、3-甲基哌啶、4-甲基哌啶、n-甲基哌啶、甲基三氯硅烷、甲基三乙氧基硅烷、甲基叔丁基醚、2-甲基四氢呋喃、2-甲基戊烷、3-甲基戊烷、2-甲基烯丙醇、甲基溴化镁[浸在乙醚中]、甲基异丙基苯、甲硫醚、甲醛溶液、甲酸、甲酸甲酯、甲酸乙酯、甲酸异丙酯、甲酸异丁酯、甲酸正丁酯、甲酸正己酯、2-甲氧基苯胺、3-甲氧基苯胺、4-甲氧基苯胺、甲氧基苯甲酰氯、2-甲氧基乙酸乙酯、间苯二甲酰氯、间苯三酚、金属铪粉、金属锰粉[含水≥25%]、金属钛粉[干的]、精蒽、肼水溶液[含肼≤64%]、酒石酸锑钾、聚乙烯聚胺、2-莰醇、糠胺、糠醛、喹啉、连二亚硫酸钠、联苯、邻氨基苯硫醇、邻苯二甲酸二异丁酯、邻苯二甲酸酐[含马来酸酐大于0。以乙醛酸为原料与原甲酸三甲酯在浓硫酸存在下合成得到二甲氧基乙酸甲酯,后者与乙酸甲酯、甲醇钠反应得到4,4’-二甲氧基乙酰乙酸甲酯。
早安小王子@TFBOYS-易烊千玺