高中化学喷泉实验创新设计
化学毕竟是一门实验学科,在实验教学中,老师的任务不应该仅仅是把实验给学生讲一遍具体操作,演示一遍之后,让同学们照葫芦画瓢的重复一下实验步骤。2.在书写电离方程式时,可以联系着溶解现象与溶解原理、物质的电离、溶液的导电性及其原理分析、化学式和离子符号的书写、化学符号及其周围数字的意义等相关知识,来理解、分析和书写即可.其中,最关键的是从化学式的哪个地方电离开来,产生相应的阴、阳离子。3.王磊、陈光巨.化学必修1、2[m],化学与生活[m],化学与技术[m],有机化学基础[m],化学反应原理[m],实验化学[m]高中化学喷泉实验,物质结构与性质[m].山东科学技术出版社, 2005,8. 1i8+)p{。
接着,正式的实验开始了,繁琐的步骤我便不说了,只是老师让我前面的同学用止水夹夹住了橡皮管。(2)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收集到的氧气体积(装置选用a、f、g),若各装置的连接顺序是:a→b→c→d高中化学喷泉实验,f装置内导管(“b”或“c”)该怎样延伸。实验1中mno2的作用是催化剂,实验2中又加入硫酸,生成气体体积增大,且为实验1中的2倍,说明二氧化锰不是催化剂,实验1中过氧化氢分解时发生反应:2h2o2 2h2o+o2↑,可知实验2中过氧化氢中氧元素全部被氧化为氧气,二氧化锰起氧化剂作用。
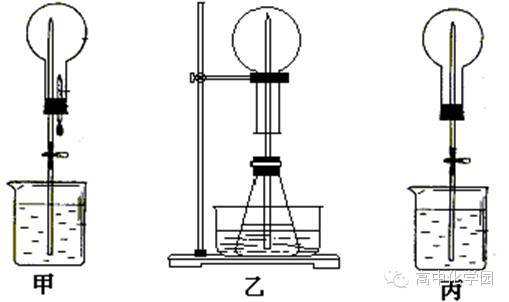
41.如图27所示,实验桌上有若干完全相同的烧瓶,烧瓶内装有质量相等、初温相同的煤油、完全相同的温度计,烧瓶内还分别装有已知阻值大小不同的电阻丝,满足实验要求的电源、滑动变阻器和开关各一个,电流表和停表各一块,导线若干。10.用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)()a.用装置甲检验溶液中是否有k+b.用装置乙制取并收集少量nh3c.用装置丙进行喷泉实验d.用装置丁加热熔融naoh固体解析:选ba项,钾的焰色反应应该透过蓝色钴玻璃观察,错误。b 某实验小组从资料上获得信息:fe3+可以氧化银单质.他们用这种方法清洗一批作了银镜反应的试管,配制了fe3+浓度相同的fecl3溶液和fe2(so4)3溶液,分别用于清洗实验. 用fecl3溶液清洗比fe2(so4)3溶液清洗得干净 他们认为fe3+氧化银单质的过程可能是一个可逆过程:fe3++ag⇌。
(6)so32- 浓溶液能与强酸反应,产生无色有刺激性气味的so2气体,该气体能使品红溶液褪色.能与bacl2溶液反应,生成白色baso3沉淀,该沉淀溶于盐酸,生成无色有刺激性气味的so2气体.。 正 4oh- - 4e - o2↑+ 2h2o 16 碱性增大,水量减少、氢氧化钠浓度增大 酸性增强,水电离出的oh-放电生成氧气和h+ 酸碱性不变化,因为硫酸钾是强酸强碱盐,浓度增大不影响溶液的酸碱性 能继续进行,因为硫酸铜溶液已转变为硫酸溶液,反应也就变成水的电解反应 v 2.8l 问题二 用惰性电极电解溶液,如何判断阴阳极产物。(3)为到净化气体的目的应使气体通过溶液,所以气体应从a通入溶液,通过溶液装置d内盛放的碳酸氢钠溶液能与混在气体中的hcl发生反应生成氯化钠、水和二氧化碳,从而除去混在气体中的hcl,反应的化学方程式为:nahco3+hcl═nacl+h2o+co2↑。

②一段时间后,拉注射器2的活塞,促进两个瓶中的气体流动.观察溴麝香草酚蓝溶液的变色情况.(阀门a和b关闭时,整个装置是密封的)。挥发油不可以用索氏提取器提取索氏提取器是一个漏斗加溶液挥发回流的2个管子.原理是下面溶液瓶中的有机溶剂(乙醇等)在加热的情况下(一般是水浴,所以这个温度不会超过100度,那么瓶中装水基本是挥发不了的,就不能使用),有机溶剂挥发成气体从粗的管子上升到索氏提取器中,由于索氏提取器上方的冷凝管作用,气体又变成液体落到索氏提取。ru(oh)4的沉淀物用3l6mhcl溶液溶解,用稀碱调节至ph为1左右加入蒸馏釜中,连接好钌的吸收系统,蒸馏釜升温至80℃,逐渐向其中加入20%的naoh溶液和20%的nabro3溶液,当检查到有ruo4气体逸出时,停止加naoh溶液而继续加入nabro3溶液,继续蒸馏,直至检验无ruo4气体,蒸馏共持续12h。