2018学年高一下学期3月月考化学试题(2)
C.直型玻璃管中发生的反应为:3CuO+2NH3 N2↑+3Cu+3H2O
N2↑+3Cu+3H2O
D.若打开K,鼓入空气,直型玻璃管中氧化铜粉末会交替出现黑色变红色,红色变黑色的现象
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:一般使用:107次加入试题篮收藏
【题文】新型纳米材料氧缺位铁酸盐(MFe2Ox),能使SO2、NO2等氧化物转化为单质。转化流程如图所示,下列有关该转化过程的叙述不正确的是
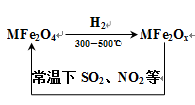
A.MFe2O4表现了氧化性
B.若MFe2Ox与SO2发生反应的物质的量之比为3:1,则x=10/3
C.在处理该废气过程中,每处理含1moINO2的废气转移电子数4NA个
D.MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应
来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:较难使用:225次加入试题篮收藏
【题文】非金属虽然种类虽然不多,但是与人类的关系密切,回忆几种常见非金属一硅、氯、硫、氮及其化合物的重要性质,回答下列问题:
(1)在无机非金属材料中,硅一直扮演着主要的角色,有下列物品或设备:①陶瓷餐具②砖瓦③水泥路桥④门窗玻璃⑤水晶镜片⑥人工制造的分子筛⑦玛瑙手镯⑧硅太阳能电池⑨石英光导纤维⑩计算机芯片。所用材料为SiO2或要用到SiO2的是_______。
A.④⑤⑦⑧⑨ B.④⑤⑦⑨ C.④⑤⑦⑨ D.①④⑤⑦⑨⑩
(2)1774年,瑞典化学家舍勒在研究软锰矿的过程中发现了氯气。高中化学喷泉实验现为了进行有关氯气的性质实验,需要4瓶容积为50mL的氯气(室温下,氯气的密度约为2.9g/L),则用舍勒的方法制取3瓶氯气理论上需要MnO2固体的质量是_____g(保留到小数点后一位,浓盐酸过量,可以补充);实际称量的MnO2固体的质量必须多于理论量,其原因是_____,由于氯气有毒,拆除装置时需要对反应装置内氯气进行处理,以下最理想的吸收剂是_____
A.NaOH溶液 B.浓氨水 C.澄清石灰水 D.水
(3)硫酸和硝酸都是重要的化工原料,在工业上可以用于制化肥、农药、炸药、盐类等。
①现以洗净的废铜屑和浓硝酸为原料,制取硝酸铜,请设计一个既能节约原料又能防止污染环境的方法(用化学方程式表示)____________。
②下列现象中硫酸所表现出的性质中含有强氧化性的是________。
A.把锌粒放入稀硫酸中时,有气体放出
B.盛有浓硫酸的烧杯敞口放置一段时间后,质量增加
C.把浓硫酸倒入润湿的蔗糖中,蔗糖变黑,且有刺激性气味气体生成
D.把木炭放入热的浓硫酸中时,有气体放出
E.在常温下可以用铁、铝制容器盛装冷的浓硫酸来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:一般使用:89次加入试题篮收藏
【题文】氯及其化合物对人类生产及生活有重要作用。
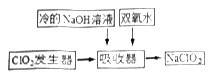
(1)氯的原子结构示意图为_______;实验室氯气的尾气处理常用NaOH溶液,请用离子方程式表示该反应:________;工业上将氯气通入冷的消石灰制取漂白粉,漂白粉的有效成分是___(填化学式)。
一辰yc系列产品有几十种型号规格,产品已成功应用于自来水、生活污水、医院污水、工业废水、自备井水、二次供水、电厂、钢铁循环水、油田污水、印染废水、造纸漂白、畜牧场、食品保鲜等多种领域,目前hy系列二氧化氯发生器在饮用水、市政污水、医院污水、食品厂、工业循环冷却水、中水回用等不同领域得到广泛的应用,积累了丰富的经验。据报道,世界上钛矿物90%以上用于生产二氧化钛白色颜料,而此产品在油漆、橡胶、塑料、造纸等工业中的应用越来越广泛。次氯酸钠主要用于漂白、工业废水处理、造纸、纺织、制药、精细化工、卫生消毒等众多领域,具体是:用于纸浆、纺织品(如布匹、毛巾、汗衫等)、化学纤维和淀粉的漂白。

(7)乙烯和水在催化剂作用下加成生成乙醇,乙醇氧化生成乙醛,乙醛在题给信息的条件下反应生成,在浓硫酸加热条件下发生消去反应生成chcho在催化剂、氧气加热条件下发生催化氧化生成和乙醇发生酯化反应,即可得物质e,合成路线为:答案 (1)(2)浓hno3和浓h2so4(3) (4)碳碳双键、酯基(5)加聚反应(6) +nc2h5oh原创总结有机合成路线设计思维导图(2016·江苏,20(5))化合物h是合成抗心律失常药物的一种中间体,可通过以下方法合成:已知:1.苯胺易被氧化请以甲苯和(ch3co)2o为原料制备,写出制备的合成路线流程图(无机试剂任用)。【板书】根据方程式判断氧化和还原能力的相对强弱:氧化性:氧化剂>氧化产物还原性:还原剂>还原产物【强调】根据氧化剂和还原剂的相对强弱,我们不但可判断某些氧化还原反应能否发生和反应的难易,而且还能判断反应进行的程度以及氧化产物、还原产物。感悟:从近3年全国i卷试题可以看出,生活中的化学、化学中的stse等基本上都是元素化合物知识的考查,广泛涉及具体物质的性质,3道选择题就涉及30多种物质的性质特点,考查到强氧化性酸与金属的反应、盐类水解与酯类水解、酸碱盐间的复分解反应、不稳定酸的分解反应、不活泼金属与盐溶液的氧化还原反应、侯氏制碱法的特殊反应、气体物质生成铵盐的化合反应、黑火药制备反应等10余种反应原理。
3.化学反应速率和化学平衡:化学反应速率,影响化学反应速率的因素(浓度、温度、催化剂),基元反应,质量作用定律,反应速率方程,反应级数,阿伦尼乌斯方程式,碰撞理论,活化能,活化分子,过渡态理论,活化能与反应速率的关系,平衡常数(实验平衡常数,标准平衡常数(kӨ)),多重平衡规则,kӨ与&delta。a′b′确定 o2/vxv=a′+b′/nrs a′ 0.42---0.53 b′ 0.188---0.114.3 活性污泥反应动力学基础 一. 概述 研究目的 {①研究反应速度和环境因素间的关系 {②对反应的机理进行研究,使反应进行控制 反应动力学方程式 {米门方程式 1913 研究酶促反应速度污泥减量微生物制剂 污泥减量微生物制剂提供商 {莫诺方程式 1942 {劳—麦方程式 1970 二. 莫诺方程式 1. 基本方程式形式 提出人:莫诺 时间: 物的培养基中 试验内容:研究微生物的增值速度与底物浓度间的关系 结果与米门方程式相同 。【解析】生物的所有生命活动都是对环境的一种适应,这个根据进化论可以证明,蒸腾作用能降低植物体的温度,避免因温度过高晒焦导致死亡,能产生向上抽力,促进水、无机盐吸收等,是对陆生环境的一种适应,同时植物的蒸腾作用能够为大气提供大量的水蒸气,使当地的空气保持湿润,使气温降低,让当地的雨水充沛,形成良性循环,因此植物的蒸腾作用能够影响周围环境的温度和湿度,是对环境的影响,d正确。
③Cl2和ClO2均能将工业废水中得CN-氧化成无毒的物质,而自身被还原为Cl-,则处理相同量的CN-所需Cl2的质量是ClO2的多少倍。______(计算结果保留一位小数)。来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:一般使用:115次加入试题篮收藏
【题文】中科院官方微信中科院之于2017年3月9日发表《一个“网红”的转化-灰霾专题》,提出灰霾细颗粒物的成因,部分分析如下图所示。
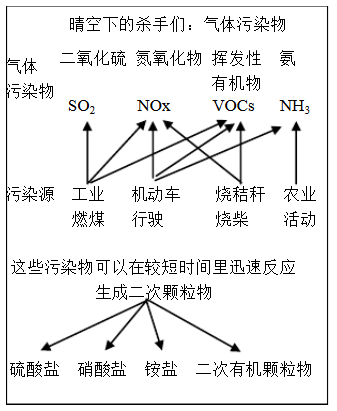
(1)根据上图信息可以看出,下列哪种污染源不产生NOx_________.
A.工业燃煤
B.机动车尾气
C.烧秸秆
D.农业活动
(2)若某地空气潮湿,且空气含有的大气污染物主要是SO2、NH3,根据上图中所举的“SO2 SO32-
SO32- 盐
盐 SO42-
SO42- 盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:_____________。
盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:_____________。
(3)当前频繁出现的雾霾天气与汽车尾气的排放有一定的关系,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。
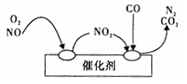
写出净化过程中的总化学方程式:________
(4)将装有amLNO和NO2混合气体的集气瓶倒立在水槽中,然后鼓入一定量O2,最终集气瓶里面剩余气体体积为bmL,则集气瓶内所得HNO3的物质的量浓度为______mol/L(不考虑集气瓶内硝酸扩散到水槽中,设气体摩尔体积为Vm)。来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:一般使用:108次加入试题篮收藏
【题文】焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂(易被氧化),某研究性学习小组为了制备少Na2S2O5,并探究SO2的某些性质,设计下图所示装置(夹持装置已略去)。请回答下列问题。

(1)向A中滴加的硫酸最好选用______(填字母)。
A.98%的浓硫酸 B.70%的硫酸 C.10%的稀硫酸
(2)打开分液漏斗旋塞,发现其中的液体不能流下,应采取的操作是___________.
(3)装入药品后,打开K1、K2、K3并从K3处通入一段时间的N2,其目的是______,N2充满装置后再关闭K1、K3,打开K2,滴入硫酸后E中有Na2S2O5晶体析出,装置E中的反应方程式为_____
(4)关闭K2、K3,打开K1,若探究SO2的漂白性,装置B应盛有_____溶液,若B中所装溶液为酸性KMnO4溶液,B中发生反应的离子方程式为______,B中紫色完全褪去后,继续滴加硫酸,则装置C中观察到的现象是__________。
由反应现象推导反应本质,验证预测的正确性 追问 追问:由上述现象,同学们得出什么结论。②利用雪地设计一个实验粗略验证这种猜想的正确性(简要写出实验步骤及判断方法).。【解题方法点拨】对于探究型实验探究,要熟悉实验探究的环节和方法,精心设计实验方案,将所学过探究物质的性质或变化规律的技巧迁移至此,进行细心地探究实验和观察现象,再通过分析实验现象,推断、总结出该物质的性质或变化规律等. 对于验证型实验探究,要熟记物质的性质或变化规律,根据给出的实验设计方案,进行实验、分析和探究,并通过观察、记录和分析的实验现象,来验证该物质的性质或变化规律等.。
仪器自选,供选择试剂:滴加酚酞的氢氧化钠溶液、氯化亚铁溶液、硫氰化钾溶液、品红溶液。
___________________________________________________。来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:一般使用:97次加入试题篮收藏
【题文】已知:X、Y分别是地壳中含量最高的金属和非金属元素的单质,D、E、F为气体,X在酸性或碱性溶液中均可与NO3-发生氧化还原反应,气体D和G反应可生成盐,气体D和A溶液反应生成白色沉淀,气体E和F在NaOH溶液中按1:1反应钠盐M,各物质转化关系如下:
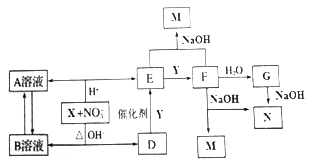
请回答下列问题:
(1)M的化学式__________。
(2)请写出D的溶液与A溶液反应的离子方程式:___________
(3)写出X在碱性条件下与NO3-反应的离子方程式:_____________
(4)标况下,若E,F的混合气体共48mL,恰好被10mL菜浓度的NaOH溶液吸收,则该NaOH溶液浓度为______mol,若反应后所得溶液中M和N的浓度之比为7:1,则原来气体中E与F的体积比为________。来源:【全国百强校】重庆市巴蜀中学2017-2018学年高一第二学期3月月考化学试题上传:2018-04-11
难度:一般使用:103次加入试题篮收藏
我会相信质监局买的是假货