⑴检查图1装置气密性的方法是 .⑵若要比较产生气体的快慢.可

根据下图回答问题。
 |
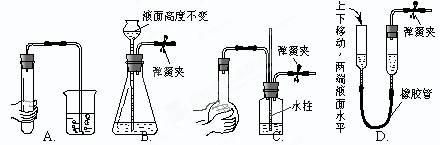
(1)仪器a的名称是 。
(2)实验室制取二氧化碳所选用的发生装置是 (填装置序号,下同),不选择装置E收集二氧化碳的原因是______________________。
(3)实验室用高锰酸钾制取氧气反应的化学方程式是 _____________________ ,
所选用的收集装置是E或 。主要的实验步骤有:①加热 ②装药品并固定
试管 ③检查装置的气密性 ④用排水法收集氧气 ⑤停止加热 ⑥将导管从水
槽中取出。正确的操作顺序是 _____________ (用序号表示)。
(1)酒精灯(2)B 二氧化碳能溶于水且与水反应(只答一点给分)
16. 加热高锰酸钾:2kmno4 加热 k2mno4 + mno2 + o2&uarr。16. 加热高锰酸钾:2kmno4 加热 k2mno4 + mno2 + o2↑。17、已知298k时,mno2 s →mno s +o2 g 的△rh 1 134.8kj·mol-1,mno2 s +mn s →2mno s 的△rh 2 -250.4kj·mol-1,则△fh mno2,s 为.【17】答:(c)a -385.2kj·mol-1。
32.(5分)32.(5分)某化学小组测定空气中氧气的体积分数。
 (1)根据右图回答问题。
(1)根据右图回答问题。
①红磷燃烧的化学方程式为__________________________________。
②若将红磷改为木炭,反应结束后降至室温,打开止水夹,烧杯
中的水不倒吸入集气瓶的原因是______________________________
 _______________________________________________。
_______________________________________________。
(2)用四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数。
反应原理为:2Na2S4+O2+2H2O 8S↓+4NaOH(氢氧化钠)。
小资料:四硫化钠(Na2S4)与氧气、水反应生成难溶于水的固体硫(S)和易溶于水
的氢氧化钠。

【实验过程】
(3)现将45gnahco3(混有khco3)固体粉末加入100ml稀硫酸,恰好完全反应后是气体全部逸出,固体粉末的质量与产生co2的体积的关系如图(该状况下,co2的密度为2g/l)所示,计算:。苏州)小明在实验室用天平和量筒测量矿石的密度,他先把托盘天平放在水平桌面上,将游码移到标尺左端的零刻度线处,发现指针在图甲位置静止,接着他将天平右端的平衡螺母向左调节,使横梁在水平位置平衡,然后他用天平测量矿石的质量,示数如图乙所示,则矿石的质量为52g.最后他用量筒测量矿石的体积,示数如图丙所示,由此可得矿石的密度为2.6×103kg/m3.。(2)有一根细而均匀的中空柱状导电材料样品如图a所示,截面为同心圆环如图b所示,在样品两端面上有焊接良好的引出导线.样品长约5cm,教师用多用电表的欧姆挡预测电阻时,选择开关置于“×10”倍率挡,其示数如图c所示,已知这种材料的电阻率为ρ,因该样品的内径太小,无法直接用长度测量工具测量.现提供下列实验器材:。
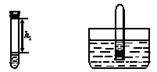
图1 图2
②将该试管插入水中(如图2所示),拔下橡胶塞,观察到__________,塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2。检查二氧化碳装置的气密性方法理论上h2∶h1= 。
③按照①和② 再重复实验2次。3次实验数据如下表所示。
再重复实验2次。3次实验数据如下表所示。
| 第1次 | 第2次 | 第3次 | |
| h1/cm | 11.0 | 11.4 | 11.6 |
| h2/cm | 8.7 | 9.1 | 9.2 |
根据第3次实验数据,计算空气中氧气的体积分数为 %(结果精确到 0.1%)。
(1)①4P + 5O 2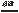 2P2O5
2P2O5
在一定温度和压强下,气体在一定量溶剂中溶解的最高量称为气体的溶解度.常用定温下1体积溶剂中所溶解的最多体积数来表示.如20℃时100ml水中能溶解1.82ml氢气,则表示为1.82ml/100ml水等.气体的溶解度除与气体本性、溶剂性质有关外,还与温度、压强有关,其溶解度一般随着温度升高而减少,由于气体溶解时体积变化很大,故其溶解度随压强增大而显著增大.关于气体溶解于液体的溶解度,在1803年英国化学家w.亨利,根据对稀溶液的研究总结出一条定律,称为亨利定律.。气体的溶解度有两种表示方法,一种是在一定温度下,气体的压强(或称该气体的分压,不包括水蒸气的压强)是1.013×10^5pa时,溶解于一体积水里,达到饱和的气体的体积(并需换算成在0℃时的体积数),即这种气体在水里的溶解度.另一种气体的溶解度的表示方法是,在一定温度下,该气体在100g水里,气体的总压强为1.013×10^5pa(气体的分压加上当时水蒸气的压强)所溶解的克数。气体的溶解度有两种表示方法,一种是在一定温度下,气体的压强(或称该气体的分压,不包括水蒸气的压强)是1.013×10^5pa时,溶解于一体积水里,达到饱和的气体的体积(并需换算成在0℃时的体积数),即这种气体在水里的溶解度.另一种气体的溶解度的表示方法是,在一定温度下,该气体在100g水里,气体的总压强为1.013×10^5pa(气体的分压加上当时水蒸气的压强)所溶解的克数.。

化,所以,当打开止水夹时水不会吸入到集气瓶中。
故答案为:漏斗中与试管中的液(水)面差保持不再变化或漏斗中的液(水)面不再下降。然后把三支试管并在一起,同时倒置过来,观察比较试管中的气泡上升速度,上升快的油粘度小,上升慢的油粘度大。4.1 将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml 烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37℃±1℃的水(或规定的溶液),调节液面高度使吊篮上升时筛网在液面下15mm处。
33.(8分)某兴趣小组同学阅读课外资料得知:很多因素都能影响过氧化氢分解速度。于是,
同学们探究影响过氧化氢分解速度的某种因素。检查二氧化碳装置的气密性方法
【实验过程】实验数据记录如下:
| 过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | MnO2的质量 | 测量数据 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9 mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16 mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31 mL |
【实验分析】
(1)过氧化氢分解的化学方程式为______________________________________。
(2)表格中的“测量数据”的指的是:相同时间内_________________________________。
(3)本实验中,测量O2体积的装置是________(填编号)。

 |
【实验结论】
在相同条件下______________________________________________。
【交流评价】
(1)甲同学提出在上述实验中测量______________同样能得出相同的结论。
 (2)乙同学提出用右图装置进行实验,通过比较_____________
(2)乙同学提出用右图装置进行实验,通过比较_____________
___________________也能达到实验目的。
【实验反思】
除了上述因素会影响过氧化氢分解速度外, ___________(写
一种)也会影响过氧化氢分解速度,你的实验方案是______________________________________________________________________。
剩我买块电池么