有关物质的转化关系如图所示.A.C都是常见的金属氧化物.B是

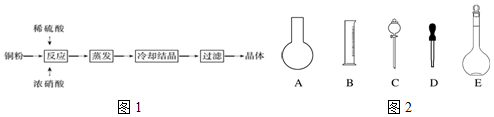
14.CuSO4•5H2O是铜的重要化合物,有着广泛的应用.如图是CuSO4•5H2O的实验室制备流程图1.

根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加少量浓硝酸(可加热),在铜粉溶解时硝酸的作用:氧化剂.

(2)根据制备原理,铜恰好完全溶解时,硝酸与硫酸的物质的量之比为2:3(假设硝酸全部还原为NO).
(3)实验室需配制质量分数为15%的CuSO4溶液480mL其密度为1.07g/mL,根据溶液的配制情况回答下列问题:如图2所示的仪器中配制溶液肯定不需要的是ABC(填序号),在配制上述溶液还需用到的玻璃仪器是烧杯、玻璃棒(填仪器名称).根据计算用托盘天平称取CuSO4•5H2O的质量为125.4g.

(4)将CuSO4•5H2O与NaHCO3按一定的比例共同投入到150ml沸水中,剧烈搅拌,冷却后有绿色晶体析出,该晶体的化学组成为Cux(OH)y(CO3)z•nH2O,实验所得的绿色晶体需充分洗涤,检验是否洗涤干净的方法是取最后一次洗涤液少许与试管中,加入盐酸酸化的BaCl2溶液,若有白色沉淀产生,则未洗净,反之洗净
为了确定晶体的化学式,某实验小组进行如下实验:

取li2o浓度为38g/l的li2so4浸出液10000ml,向其加入ca(oh)2调节ph =7,过滤,再向滤液中加入iosog氢氧化钠,充分搅拌使其完全溶解,然后在搅拌状况 下将其冷至_3°c,当溶液中s042_浓度在35g/l时,将其过滤分离,得到lioh溶液和 na2so4 · ioh2o固体。二氧化碳密度为1.977g/ml,熔点-56.6℃(226.89千帕——5.2大气压),沸点-78.5℃(升华).临界温度31.1℃.常温下7092.75千帕(70大气压)液化成无色液体.液体二氧化碳密度1.1克/厘米3.液体二氧化碳蒸发时或在加压冷却时可凝成固体二氧化碳,俗称干冰,是一种低温致冷剂,密度为1.56克/厘米3.二氧化碳能溶于水,20℃时每100体积水可溶88 体积二氧化碳,一部分跟水反应生成碳酸.化学性质稳定,没有可燃性,一般不支持燃烧,但活泼金属可在二氧化碳中燃烧,如点燃的镁条可在二氧化碳中燃烧生成氧化镁和碳.二氧化碳是酸性氧化物,可跟碱或碱性氧化物反应生成碳酸盐.跟氨水反应生成碳酸氢铵.无毒、但空气中二氧化碳含量过高时,也会使人因缺氧而发生窒息.绿色植物能将二氧化碳跟水在光合作用下合成有机物.二氧化碳可用于制造碳酸氢铵、小苏打、纯碱、尿素、铅白颜料、饮料、灭火器以及铸钢件的淬火.二氧化碳在大气中约占总体积的0.03%,人呼出的气体中二氧化碳约占4%.实验室中常用盐酸跟大理石反应制取二氧化碳,工业上用煅烧石灰石或酿酒的发酵气中来获得二氧化碳.。(4)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出.你认为“全部溶解”的原因可能是.。
b.称取等质量的晶体,灼烧至完全分解,得到2.400g残余固体,通过计算确定晶体的化学式Cu3(OH)2(CO3)2•H2O或Cu(OH)2•2CuCO3•H2O.
19、向 0.10 mol.dm-3hcl溶液中通h2s气体至饱和 (0.10 mol.dm-3 ),溶液中 s2-浓度为(h2s: ka 1 = 9.1×10-8 ka 2 = 1.1×10-12 ( )。l-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的ph=8时,c(cu2+)=________________mol•。l-1硫酸铜溶液中通入过量h2s气体,使cu2+完全沉淀为cus,此时溶液中的h+浓度是_______________mol•。
说明人家觉得用这条船到南海正好